In tema di Maculopatie
- Complicanze della pdt e autofluorescenza
- Corioretinopatia Sierosa Centrale
- DMS : DEGENERAZIONE MACULARE SENILE
- Edema Maculare ed occlusioni venose retiniche
- Foro Maculare
- Maculopatia Diabetica
- Maculopatia Miopica
- Maculopatia Senile: niente vitamine
- Tomografia a coerenza ottica
- Terapie possibili e disponibili sul mercato
- Up-to-date: microperimetria e applicazioni nella gestione delle patologie maculari
- Age-Related Macular Degeneration Guidelines for Management
- The intravitreal use of bevacizumab (avastin) in age related macular degeneration
- Maximising Capacity in AMD Services
- Pucker Maculare
Corioretinopatia Sierosa Centrale
di Felice Cardillo PiccolinoDefinizione - cenni storici
La Corioretinopatia Sierosa Centrale (CSC) è una malattia caratterizzata da un distacco sieroso idiopatico del neuroepitelio al polo posteriore prodotto dal passaggio di fluido dalla coroide nello spazio sottoretinico attraverso un difetto dell'epitelio pigmentato.Dalla prima descrizione da parte di von Graefe nel 1866 ("recurrent central retinitis") è stata oggetto di numerose descrizioni ed interpretazioni.
Negli anni '60 Maumenee e Gass diedero un importante contributo alla comprensione della malattia descrivendone il caratteristico quadro fluorangiografico.
Maumenee individuò la sorgente del fluido sottoretinico nel leakage attraverso l'epitelio pigmentato.
Gass precisò ulteriormente le caratteristiche angiografiche della malattia dandole la denominazione di "corioretinopatia sierosa centrale".
Gass suggerì che un'essudazione nella coroide possa produrre prima un piccolo distacco dell'epitelio pigmentato e poi una lesione di barriera e passaggio di fluido nello spazio sottoretinico.
Epidemiologia - Fattori di rischio
La CSC è classicamente considerata una malattia che predilige il sesso maschile (85%), con età di insorgenza fra i 30 e i 50 anni.È meno frequente nella razza nera e può presentarsi in forme particolarmente gravi negli asiatici.
Una personalità di tipo A sembra poter favorire l'insorgenza della CSC.
Le persone con questo tipo comportamentale sono particolarmente attive, hanno atteggiamento competitivo, sono facili allo stress, hanno sensazione di dover affrontare situazioni di urgenza ("hurry sickness").
Costituiscono anche fattore di rischio condizioni che comportino un aumento del cortisolo ematico come gravidanza, sindrome di Cushing, lupus eritematoso sistemico, emodialisi, trapianto di organi e naturalmente l'assunzione di corticosteroidi.
Vi sono diverse descrizioni, soprattutto recenti, di CSC in donne.
Nel caso delle donne l'età di insorgenza è spesso superiore ai 50 anni. Si trova spesso presente una condizione di ipercortisolismo endogeno o esogeno.
Caratteristiche cliniche - Fluorangiografia
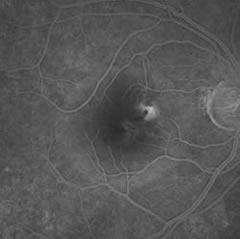 L'esordio è solitamente subdolo ed i sintomi sono monolaterali.
L'esordio è solitamente subdolo ed i sintomi sono monolaterali.Nell'occhio controlaterale si possono riscontrare lesioni extrafoveali sintomatologicamente silenti.
La sintomatologia consiste in visione appannata, presenza di scotoma centrale relativo e metamorfopsia.
La visione è più scura, i colori più sbiaditi, l'acutezza visiva raramente raggiunge valori inferiori ai 5/10 e migliora con lenti positive.
All'oftalmoscopia ed alla biomicroscopia si osserva tipicamente un sollevamento sieroso della retina neurosensoriale localizzato alla regione maculare.
A livello dell'epitelio pigmentato si possono a volte notare piccoli spot multipli, giallastri, che consistono in precipitati proteinacei e caratterizzano la fase di risoluzione del processo essudativo.
Vi sono casi non frequenti in cui è presente un'essudazione biancastra all'interno del distacco, rappresentata da fibrina. È osservabile soprattutto nei casi di CSC associata a gravidanza o ad assunzione di corticosteroidi.
La presenza di fibrina è segno che esiste un'alterazione importante della permeabilità della coroide tale da permettere la fuoriuscita di molecole grosse come il fibrinogeno.
Uno o più distacchi sierosi dell'epitelio pigmentato possono associarsi al sollevamento sieroso del neuroepitelio, all'interno o all'esterno di questo. Possono osservarsi anche indipendentemente dalla presenza di un distacco del neuroepitelio.
Alla fluorangiografia è tipico il rilievo di un "leakage" focale o multifocale a livello dell'epitelio pigmentato retinico. Lesioni recenti danno una diffusione del colorante a filo di fumo. Col perdurare del processo la diffusione appare più lenta e a macchia d'inchiostro.
Gli eventuali piccoli distacchi dell'epitelio pigmentato risultano iperfluorescenti e chiaramente rilevabili.
Esistono casi di CSC con quadro clinico e compromissione funzionale particolarmente gravi. Sono caratterizzati da distacchi retinici ampi, bollosi, che possono estendersi alla periferia inferiore, con leakage fluoresceinico intenso e multifocale. Sono spesso forme bilaterali e tendenti alla recidiva.
La somministrazione di corticosteroidi può essere alla base di questi casi più gravi di CSC.
La malattia al primo episodio si risolve in genere spontaneamente in 3-4 mesi con un eccellente recupero funzionale.
Tende però a recidivare (45-50% dei casi) e può diventare cronica per il formarsi di aree di persistente scompenso dell'epitelio pigmentato.
L'ipertensione sistemica sembra essere un fattore favorente la cronicizzazione.
Nei casi di CSC cronica si possono osservare aree più o meno estese di atrofia dell'epitelio pigmentato e, nelle forme più avanzate, degenerazione maculare cistoide, essudati lipidici, fibrosi sottoretinica e neovascolarizzazione coroideale
Le alterazioni del neuroepitelio e dell'epitelio pigmentato maculare si traducono in danni gravi ed irreversibili della visione centrale.
I pazienti con recidive multiple, distacchi persistenti e diffuso interessamento dell'epitelio pigmentato retinico sono a più alto rischio di compromissione visiva grave.
Nella CSC cronica la fluorangiografia mostra aree indefinite di "staining" dove esiste scompenso dell'epitelio pigmentato e passaggio di fluido nello spazio sottoretinico. Iperfluorescenza trasmessa dalla coroide si rileva nelle zone di epiteli pigmentato atrofico che si sviluppano intorno ed inferiormente alle aree di scompenso per la persistenza cronica di liquido sottoretinico.
Angiografia con verde di indocianina
Negli anni '90 l'angiografia con verde di indocianina ha fornito rilievi che caratterizzano ulteriormente la CSC.Ha fornito anche informazioni importanti per chiarire le basi fisiopatologiche della malattia.
Il rilievo più interessante è la diffusione del colorante in aree della coroide che pertanto si dimostrano iperpermeabili. Queste aree di iperpermeabilità coroideale si osservano in corrispondenza delle alterazioni di barriera e dei distacchi dell'epitelio pigmentato, ma anche in zone dove l'epitelio pigmentato appare integro.
I distacchi dell'epitelio pigmentato sono inizialmente iperfluorescenti e dopo alcuni minuti si svuotano del colorante mantenendo una iperfluorescenza residua lungo il bordo.
È stato osservato che l'iperpermeabilità della coroide precede le alterazioni dell'epitelio pigmentato e persiste anche dopo la riparazione delle lesioni di barriera.
Un'abnorme condizione di iperpermeabilità di alcune zone della coroide caratterizza quindi i pazienti con CSC, sia nei momenti di attività che di inattività della malattia.
Tomografia ottica a radiazione coerente (OCT)
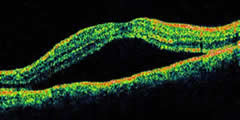 L'OCT è una tecnica diagnostica non invasiva che può essere utile per
monitorare in modo obiettivo e misurabile il sollevamento retinico maculare nel follow-up dei pazienti con CSC.
L'OCT è una tecnica diagnostica non invasiva che può essere utile per
monitorare in modo obiettivo e misurabile il sollevamento retinico maculare nel follow-up dei pazienti con CSC.È in grado di evidenziare anche minimi distacchi del neuroepitelio non apprezzabili all'osservazione biomicroscopica.
Pertanto è di particolare utilità nelle forme croniche in cui spesso esistono distacchi sierosi subclinici.
L'OCT rende anche evidenti quelle alterazioni strutturali retiniche (alterazioni degenerative e atrofia dei fotorecettori, degenerazione cistoide) che sono alla base del mancato recupero funzionale dopo eventuale risoluzione del distacco.
Diagnosi differenziale
Merita un cenno la possibilità di interpretare come CSC cronica quadri particolari di vasculopatia coroideale polipoide.Questo particolare tipo di neovascolarizzazione coroideale può associarsi a fenomeni di atrofia dell'epitelio pigmentato dando luogo a quadri fluoroangiografici che simulano una CSC cronica. L'angiografia con verde di indocianina è in genere dirimente rivelando le caratteristiche teleangectasie sottoretiniche che caratterizzano la vasculopatia coroideale polipoide.
Trattamento
Nessun trattamento medico si è dimostrato finora utile per la CSC.I corticosteroidi per via sistemica hanno dimostrato di peggiorare la CSC. Altre terapie suggerite come beta-bloccanti ed acetozolamide si sono rivelate inefficaci.
Numerosi studi hanno riportato effetti benefici della fotocoagulazione laser nel trattamento della CSC.
La maggior evidenza è che la fotocoagulazione diretta del punto di perdita a livello dell'epitelio pigmentato abbrevia la fase acuta della malattia.
Considerando la buona prognosi che la CSC ha in gran parte dei pazienti, il trattamento laser dovrebbe essere eseguito nei seguenti casi:
- persistenza di distacco maculare dopo 2 mesi;
- progressivo peggioramento visivo;
- leakage extrafoveale (almeno 300 µm dal centro maculare);
- episodi ricorrenti;
- variante grave di CSC.
La fotocoagulazione laser ha dei limiti nelle forme croniche di CSC in cui il fluido proviene da zone mal definite di scompenso dell'epitelio pigmentato.
L'applicazione di spot laser a griglia o confluenti in tali aree è spesso inefficace.
In queste forme può trovare applicazione la terapia fotodinamica.
Il trattamento guidato dall' angiografia con verde di indocianina è mirato a ridurre la per fusione nelle aree di alterata permeabilità coroideale da cui proviene il fluido sottoretinico.
Concetti patogenetici attuali
La CSC è stata per lungo tempo considerata una malattia interessante primitivamente l'epitelio pigmentato retinico.Si è ipotizzata un'alterazione del metabolismo focale o diffusa delle cellule epiteliali retiniche responsabile di inversione del movimento del fluido attraverso di esse o di riduzione della loro capacità di pompa in direzione della coroide.
Dai primi anni '90 i rilievi angiografici con il verde di indocianina hanno decisamente fatto rivolgere l'attenzione sul ruolo della coroide nella CSC.
È indubbio ormai che alla base della malattia vi sia una condizione di iperpermeabilità in alcuni distretti vascolari della coroide.
L'essudazione coroideale produrrebbe occasionalmente l'alterazione di barriera dell'epitelio pigmentato retinico e il conseguente passaggio di fluido nello spazio sottoretinico.
Rimane da chiarire come si instauri l'iperpermeabilità coroideale.
Il ruolo di uno stimolo adrenergico trova credito nell'associazione della malattia con stress e personalità di tipo A che comportano un aumento dei livelli ematici di catecolamine.
È supportato anche da osservazioni sperimentali di modelli animali di CSC creati con iniezione in vena di epinefrina. Nella coroide vi sono recettori ß2-adrenergici il cui stimolo produce vasodilatazione ed aumento del flusso ematico.
Negli anni recenti è diventato sempre più evidente il ruolo dei corticosteroidi nel favorire l'insorgenza di episodi di CSC o nell'aggravarne il decorso.
Elevati livelli ematici di cortisolo, influenzando la produzione di ossido di azoto, prostaglandine e radicali liberi, alterano indirettamente i processi di autoregolazione del flusso ematico coroideale.
Nè può derivare un aumento della pressione ematica nella coriocapillare, l'iperpermeabilità e l'essudazione.
Degenerazione Maculare Senile (DMS)
 La degenerazione maculare senile è nel mondo occidentale la prima causa di cecità legale tra la popolazione sopra
i 60 anni d'età.
La degenerazione maculare senile è nel mondo occidentale la prima causa di cecità legale tra la popolazione sopra
i 60 anni d'età.La DMS viene diagnosticata spesso casualmente dall'oculista nel corso di comuni visite di controllo in pazienti adulti che accusano diminuzione visiva generica, con richiesta di nuove lenti soprattutto per vicino, per la lettura, trovando difficoltà più importanti per la distanza ravvicinata.
Spesso non sono ancora presenti i sintomi più eclatanti della malattia, come la distorsione delle immagini o lo scotoma centrale, descritto come una macchia nera sulla carta della lettura.
L'evoluzione di tale malattia è il più delle volte lenta facendo quasi sempre mantenere l'autosufficienza dentro le mura domestiche, per svolgere le semplici azioni quotidiane autonomamente. Tale affermazione è vera se si tiene conto che la forma più frequente di DMS è quella secca che colpisce il 15,6% della popolazione tra i 43 e 86 anni, meno invalidante per la funzione visiva, mentre quella umida, o più propriamente neovascolare, colpisce nella stessa fascia d'età solo con una frequenza dell' 1,2%, ma è molto più aggressiva.
A fronte della modesta frequenza di quest'ultima forma, essa quindi costituisce la principale causa di diminuzione visiva e di cecità legale nella popolazione occidentale, portando ad ampie e distruttive cicatrici al polo posteriore.
 IRCCS Fondazione G.B. Bietti per lo Studio e la Ricerca in Oftalmologia
IRCCS Fondazione G.B. Bietti per lo Studio e la Ricerca in Oftalmologiapresenta:
Linee Guida Italiane per la Degenerazione Maculare Legata all'Età
L'obiettivo principale di queste Linee Guida è stato quello di elaborare raccomandazioni supportate da evidenze cliniche per il trattamento della Degenerazione Maculare Legata all'Età (DMLE), destinate agli operatori sanitari italiani del settore oftalmologico.
Si è ritenuto inoltre di dover introdurre uno schema di percorso diagnostico mirante ad un'adeguata schematizzazione delle fasi che preludono alla scelta terapeutica.
Sintomi
 Il sintomo caratteristico e iniziale della degenerazione maculare è la percezione alterata e distorta delle immagini
(metamorfopsie) seguita da una riduzione graduale e progressiva della visione centrale.
Il sintomo caratteristico e iniziale della degenerazione maculare è la percezione alterata e distorta delle immagini
(metamorfopsie) seguita da una riduzione graduale e progressiva della visione centrale. Anche i colori sembrano meno brillanti.
Poiché la visione centrale è compromessa, risulta impossibile la lettura in quanto le lettere su cui viene fissata l'attenzione appaiono confuse e distorte.
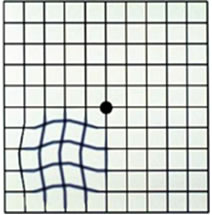
 Tipica è la distorsione delle linee
dritte (i bordi delle piastrelle del pavimento possono sembrare ondulati, il profilo di
una casa appare distorto).
Tipica è la distorsione delle linee
dritte (i bordi delle piastrelle del pavimento possono sembrare ondulati, il profilo di
una casa appare distorto).Può accadere che vengano percepite delle macchie grigie nel campo visivo o che le dimensioni di determinati oggetti appaiano diverse a seconda dell'occhio con cui si guardano.
Il sintomo tipico allo stadio terminale della maculopatia è lo scotoma (area di visione ridotta o assente nel campo visivo) centrale: la perdita della visione centrale diventa completa per cui non è possibile vedere nel punto in cui si fissa lo sguardo.
Anche nei casi più gravi, la degenerazione maculare non provoca totale cecità in quanto la visione paracentrale e laterale non è compromessa.
Prevenzione ed interventi
La terapia fotodinamica ( PDT ) introdotta da qualche tempo ha dato una speranza di trattamento a tele, forma neovascolare che quasi sempre è localizzata in area foveale o iuxta-foveale, dove la tradizionale terapia con laser argon non può essere effettuata.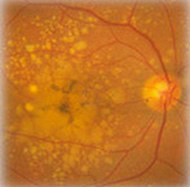
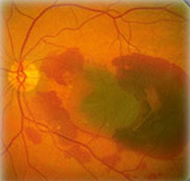 Le nuove terapie anti-angiogeniche,di recente introduzione, si spera possano dare più certe
risposte a tale invalidante malattia.
Le nuove terapie anti-angiogeniche,di recente introduzione, si spera possano dare più certe
risposte a tale invalidante malattia.L'uso combinato di più terapie, anti-angiogenica, fotodinamica e di altre terapie ancora in fase sperimentale, potranno in futuro permettere di combattere meglio e con maggior efficacia l'aggressività delle membrane neovascolari nella DMS umida.
Come sempre una più efficace risposta si può avere con la prevenzione che inizia effettuando regolarmente controlli oculisti periodici dopo i 40 anni d'età.
L'uso di farmaci antiossidanti e la protezione dai raggi ultravioletti restano fondamentali in tale malattia cronica della
retina centrale.
Si è accertato con ampia casistica che l'uso di tali presidi farmacologici sono vantaggiosi nel frenare l'evoluzione della DMS ed alcune volte a far mantenere inalterata nel tempo la capacità visiva dei pazienti.
 La protezione dai raggi solari con lenti filtranti,
la componente ultravioletta della luce solare (UVA, UVB) resta un
cardine altrettanto fondamentale nella prevenzione di tale patologia.
La protezione dai raggi solari con lenti filtranti,
la componente ultravioletta della luce solare (UVA, UVB) resta un
cardine altrettanto fondamentale nella prevenzione di tale patologia.
L'uso costante delle lenti solari quando si esce di casa dovrebbe essere presa come un'abitudine, come mettere la cintura di sicurezza in auto.
Nella diagnosi di DMS già l'esame del fondo oculare è indicativo, ma si rendono spesso necessari più fini accertamenti.
Fino a qualche anno fa solo la fluoroangiografia poteva chiarire le varie forme di DMS e suggerire un eventuale trattamento laser.
In seguito la fluoro con verde di indocianina ha ampliato le conoscenze delle forme umide, permettendo il trattamento con PDT delle forme centrali, quasi sempre invalidanti.
Oggi l'OCT, tomografia ottica a radiazione coerente, e specialmente l'OCT status di ultima generazione, permette in modo non invasivo e con grande precisione e ripetitività di studiare i vari strati retinici e quindi capire meglio questa patologia.
Anche in questo caso l'uso combinato di più metodiche può aiutare la diagnosi nei casi più complicati e difficili, comprendere meglio l'evoluzione della malattia e prendere le migliori decisioni terapeutiche.
Si è accertato con ampia casistica che l'uso di tali presidi farmacologici sono vantaggiosi nel frenare l'evoluzione della DMS ed alcune volte a far mantenere inalterata nel tempo la capacità visiva dei pazienti.
 La protezione dai raggi solari con lenti filtranti,
la componente ultravioletta della luce solare (UVA, UVB) resta un
cardine altrettanto fondamentale nella prevenzione di tale patologia.
La protezione dai raggi solari con lenti filtranti,
la componente ultravioletta della luce solare (UVA, UVB) resta un
cardine altrettanto fondamentale nella prevenzione di tale patologia.L'uso costante delle lenti solari quando si esce di casa dovrebbe essere presa come un'abitudine, come mettere la cintura di sicurezza in auto.
Nella diagnosi di DMS già l'esame del fondo oculare è indicativo, ma si rendono spesso necessari più fini accertamenti.
Fino a qualche anno fa solo la fluoroangiografia poteva chiarire le varie forme di DMS e suggerire un eventuale trattamento laser.
In seguito la fluoro con verde di indocianina ha ampliato le conoscenze delle forme umide, permettendo il trattamento con PDT delle forme centrali, quasi sempre invalidanti.
Oggi l'OCT, tomografia ottica a radiazione coerente, e specialmente l'OCT status di ultima generazione, permette in modo non invasivo e con grande precisione e ripetitività di studiare i vari strati retinici e quindi capire meglio questa patologia.
Anche in questo caso l'uso combinato di più metodiche può aiutare la diagnosi nei casi più complicati e difficili, comprendere meglio l'evoluzione della malattia e prendere le migliori decisioni terapeutiche.
Cure
La degenerazione maculare è una malattia della retina non curabile.
Nel caso della degenerazione maculare secca è possibile aiutare concretamente la capacità visiva residua utilizzando ausilii ottici e ricorrendo all'insegnamento di specialisti in ipovisione, imparando a sfruttare la capacità visiva periferica.
La degenerazione maculare umida può compromettere seriamente la capacità visiva: se diagnosticata in tempo il trattamento laser può rallentare il decorso della malattia.
Nel caso della degenerazione maculare secca è possibile aiutare concretamente la capacità visiva residua utilizzando ausilii ottici e ricorrendo all'insegnamento di specialisti in ipovisione, imparando a sfruttare la capacità visiva periferica.
La degenerazione maculare umida può compromettere seriamente la capacità visiva: se diagnosticata in tempo il trattamento laser può rallentare il decorso della malattia.
- Fotocoagulazione con Laser Termico: permette di fotocoagulare i vasi retinici anomali individuati in precedenza con l'esame fluroangiografico: il raggio laser (green) raggiunge le aree sottoretiniche e distrugge i neovasi. Con l'utilizzo del laser la vista non migliora, si interrompe solamente la fuoriuscita di liquido dai neovasi. In casi estremamente selezionati le membrane neovascolari possono essere rimosse chirurgicamente. Solitamente il beneficio ottenuto attraverso questi interventi è modesto e non è esente da rischi poiché si opera su una zona della retina estremamente vulnerabile.
- Terapia Fotodinamica con Verteporfina: è una tipologia di trattamento laser molto
complesso che richiede personale altamente specializzato operante in strutture adeguate. Ampiamente studiata nel campo
dell'oncologia per il trattamento dei tumori dermatologici, la terapia fotodinamica permette di distruggere la membrana
neovascolare maculare attraverso l'iniezione endovenosa di una sostanza farmacologia fotosensitiva che è attivata
mediante il trattamento laser.
La verteporfina svolge una potente azione citotossica legata all'induzione di una trombosi intraluminale con conseguente eliminazione di apporto sanguigno al tessuto patologico.
La sostanza si accumula selettivamente nelle cellule endoteliali dei neovasi.
La sua attivazione avviene con l'applicazione di un raggio laser utilizzato sulle aree da trattare, di lunghezza d'onda pari al picco di assorbimento della sostanza stessa (689 nm).
Il raggio laser utilizzato è di tipo non termico e di conseguenza non provoca danni alla retina sovrastante. La sicurezza, l'efficacia e la selettività di questa terapia sono state dimostrate attraverso numerosi studi sperimentali scientifici.
La terapia combinata:
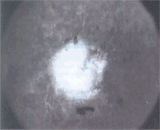 La terapia combinata (terapia fotodinamica e triamcinolone intravitreale) di recente introduzione è ancora in fase
sperimentale e per i suoi numerosi potenziali effetti avversi la diffusione su larga scala potrebbe essere limitata.
Tale terapia consiste nell'associare alla terapia fotodinamica una iniezione intravitreale di triamcinolone
(corticosteroide) che genera una diminuzione della componente infiammatoria della lesione neovascolare, potenziata
dall'azione antiangiogenetica già riconosciuta ai corticosteroidi.
La terapia combinata (terapia fotodinamica e triamcinolone intravitreale) di recente introduzione è ancora in fase
sperimentale e per i suoi numerosi potenziali effetti avversi la diffusione su larga scala potrebbe essere limitata.
Tale terapia consiste nell'associare alla terapia fotodinamica una iniezione intravitreale di triamcinolone
(corticosteroide) che genera una diminuzione della componente infiammatoria della lesione neovascolare, potenziata
dall'azione antiangiogenetica già riconosciuta ai corticosteroidi.
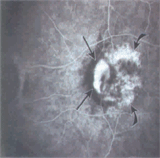 Attualmente l'attenzione si sta rivolgendo anche verso le terapie farmacologiche mirate all'inibizione del processo di
angiogenesi che sta alla base della degenerazione maculare umida.
Si tratta di molecole inibitrici del VEGF (vascular endothelial factor o fattore vascolare endoteliale),
una proteina che sembra giocare un ruolo importante nella crescita di vasi anomali a livello maculare.
Attualmente l'attenzione si sta rivolgendo anche verso le terapie farmacologiche mirate all'inibizione del processo di
angiogenesi che sta alla base della degenerazione maculare umida.
Si tratta di molecole inibitrici del VEGF (vascular endothelial factor o fattore vascolare endoteliale),
una proteina che sembra giocare un ruolo importante nella crescita di vasi anomali a livello maculare.Attualmente il VEGF è il più studiato fattore di crescita responsabile di neovascolarizzazione in vari tessuti.
Ausili ottici
 Le persone affette da degenerazione maculare dispongono di una visione periferica sufficiente per saper affrontare la vita
di tutti i giorni senza l'aiuto di altri.
Le persone affette da degenerazione maculare dispongono di una visione periferica sufficiente per saper affrontare la vita
di tutti i giorni senza l'aiuto di altri.Ciò nonostante esse faticano a leggere l'ora sull'orologio, a decifrare un cartello stradale, a riconoscere la destinazione dell'autobus: ciò che richiede capacità visiva centrale diventa per loro molto difficile da realizzare.
Tutte le attività che richiedono una buona capacità di risoluzione (leggere, guidare) esigono una macula integra; nelle persone affette da degenerazione maculare tutto ciò che viene guardato appare sfumato.
Le parti della retina distrutte non si possono sostituire né rinnovare. La degenerazione maculare riguarda però soltanto una piccola parte della retina.
Se si riuscisse ad ingrandire l'immagine da guardare in modo che essa oltrepassi la parte di macula carente e venga proiettata sul resto della retina, l'occhio dovrebbe riuscire a distinguerla.
Ciò è possibile mediante l'uso di ausili ottici, di sistemi di ingrandimento che utilizzano lenti particolari.
Per stabilire quale sia l'ausilio più adeguato, ogni persona con degenerazione maculare dovrebbe rivolgersi ad uno specialista in ipovisione. Tra gli ausili ingrandenti possono rivelarsi utili sia occhiali da lettura più forti sia occhiali con lenti telescopiche o con lenti di ingrandimento. Se ciò non fosse sufficiente si può ricorrere all'apparecchio di lettura televisivo a circuito chiuso, un sistema che è in grado di rappresentare l'oggetto da guardare o il testo da leggere su uno schermo e nella grandezza necessaria.
Prevenzione
Esistono fattori di rischio associati in modo significativo alla degenerazione maculare come ad altre patologie circolatorie. È importante controllare:- la pressione arteriosa
- la concentrazione del glucosio
- la concentrazione del colesterolo
Possono essere efficaci per la circolazione retinica i farmaci "vasoprotettori"; utili sono anche vitamine
(in particolare A, E e C) e minerali assunti a dosaggi terapeutici.
La degenerazione maculare può essere rallentata nella sua evoluzione se colta nelle fasi precoci. Spesso il paziente non riconosce i sintomi della degenerazione maculare se presenti in un solo occhio perché l'altro supplisce alla visione dei dettagli. Quando anche l'altro occhio è colpito può essere troppo tardi per qualunque trattamento.
Perciò è importante abituarsi, dopo i 40 anni, a visite periodiche di controllo a scopo preventivo. torna al menù
La degenerazione maculare può essere rallentata nella sua evoluzione se colta nelle fasi precoci. Spesso il paziente non riconosce i sintomi della degenerazione maculare se presenti in un solo occhio perché l'altro supplisce alla visione dei dettagli. Quando anche l'altro occhio è colpito può essere troppo tardi per qualunque trattamento.
Perciò è importante abituarsi, dopo i 40 anni, a visite periodiche di controllo a scopo preventivo. torna al menù
Edema maculare ed occlusioni venose retiniche
di Maurizio Battaglia Parodi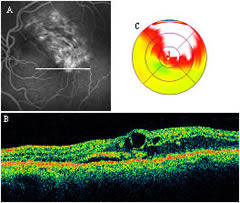 Le occlusioni venose retiniche costituiscono un gruppo di malattie vascolari retiniche piuttosto comuni che sono in grado
di determinare un severo deterioramento della funzione visiva.
Le occlusioni venose retiniche costituiscono un gruppo di malattie vascolari retiniche piuttosto comuni che sono in grado
di determinare un severo deterioramento della funzione visiva.Mediante la medesima definizione di occlusioni venose retiniche ci si riferisce in realtà ad un gruppo eterogenee di affezioni che presentano patogenesi, aspetti clinici, decorso e complicanze diverse.
In generale il danno funzionale è principalmente legato allo sviluppo di edema maculare (EM), maculopatia ischemica, o emorragie vitreali secondarie a neovascolarizzazioni retiniche o papillari.
La patogenesi dell'EM secondario ad occlusione venosa retinica dipende dagli effetti combinati di diversi fattori quali: rottura della barriera emato-retinica, aderenza vitreo-maculare e sviluppo di membrane epiretiniche.
Vi sono caratteristiche peculiari nell'EM successivo ad occlusione venosa retinica che possono essere riassunte in:
- Presenza di leakage capillare
- Scarsità o assenza di dilatazioni microaneurismatiche
- Scarsità di essudati duri
- Elevata età dei pazienti affetti
- Coinvolgimento variabile della rete capillare perifoveale
- Mancanza di corrispondenza tra aspetto biomicroscopico ed agiografico.
Prendendo in considerazione l'Occlusione Venosa Retinica Centrale, la prevalenze dell'EM non
è stata ancora definita, ma il Central Vein Occlusion Study Group ha evidenziato come tale affezione possa determinare
un profondo deterioramento dell'acuità visiva, che purtroppo non beneficia di un trattamento laser a griglia.
Infatti il trattamento laser a griglia assicura un riassorbimento dell'EM senza determinare un miglioramento della funzione visiva.
La prevalenza di EM secondario ad Occlusione Venosa Retinica di Branca è stato riportata tra il 48% ed il 67%.
Inoltre lo studio multicentrico del Branch Vein Occlusion Study Group ha provato che il trattamento laser a griglia è in grado di ridurre l'EM e migliorare l'acuità visiva.
In tal modo il trattamento laser a griglia è indicato per l'EM associato ad Occlusione Venosa Retinica di Branca, ma non per l'EM associato ad Occlusione Venosa Retinica Centrale.
Sono stati pertanto proposti ed analizzati approcci terapeutici alternativi per risolvere l'EM, quali la creazione di una anastomosi corioretinica mediante laser, l'impiego di attivatore del plaminogeno tissutale, la decompressione chirurgica del nervo ottico, la vitrectomia, l'emodiluizione e l'iniezione intravitreale di triamcinolone acetonide.
La formazione di una anastomosi chorioretinica laser-indotta è stata prospettata come una possibile soluzione per by-passare il vaso venoso centrale occluso in forme di occlusione venosa retinica centrale non-ischemiche, in modo da ridurre l'ostacolo al deflusso venoso. Una anastomosi funzionalmente valida può essere ottenuta in percentuale compresa tra il 33 ed il 63% ed è associata ad un variabile recupero visivo. Sfortunatamente questo approccio è gravato da possibili complicanze, alcune delle quali molto severe, che possono verificarsi fino al 67% dei casi.
La somministrazione per via sistemica di attivatore del plasminogeno tissutale può causare gravi complicanze generali e non è stata quindi utilizzata nella comune pratica clinica.
La sua iniezione intravitreale al fine di dissolvere il trombo, evitando le complicanze sistemiche, può invece portare ad un significativo miglioramento visivo in casi selezionati. Più recentemente alcuni autori hanno tentato di applicare direttamente la molecola sul vaso venoso occluso per mezzo di una cannulazione diretta di una branca retinica, riportando interessanti risultati.
Il razionale alla base della decompressione chirurgica del nervo ottico consiste nel concetto che una riduzione della costrizione che grava sulla vena centrale retinica può favorire il deflusso venoso, permettendo una rapido riassorbimento di emorragie retiniche ed EM con miglioramento della microcircolazione retinica.
Recentemente sono stati presentati interessanti risultati ottenuti mediante la neurotomia ottica radiale, che mira ad una decompressione sclerale attraverso un approccio per via vitreale.
L'aderenza vitreo-maculare gioca un ruolo fondamentale nella complessa patogenesi dell'EM.
Alcuni tentativi di ridurre la trazione vitreale sulla macula mediante vitrectomia del polo posteriore in forme di occlusione venosa retinica centrale con EM persistente, hanno portato a risultati incoraggianti.
Il principio base dell'emodiluizione nelle occlusioni venose retiniche si fonda sull'abbassamento dell'ematocrito per ottenere una riduzione della viscosità ematica al fine di migliorare la microcircolazione e la per fusione capillare retinica.
Diverse ricerche hanno riferito positivi risultati clinici e funzionali grazie all'emodiluizione.
In particolare, è stata descritto un incremento della acuità visiva insieme ad un miglioramento sia dei parametri emodinamici (tempo arterovenoso, velocità arteriosa media) che emoreologici (viscosità del plasma, ematocrito, fibrinogeno, aggregazione eritrocitaria).
Anche l'iniezione intravitreale di triamcinolone acetonide ha portato a risultati interessanti.
Sia l'iniezione di alti (20-25 mg), che di bassi dosaggi (4 mg) sembra in grado di promuovere la risoluzione dell'EM secondario ad occlusioni venose retiniche, come dimostrato dalla riduzione dello spessore retinico mediante tomografia a coerenza ottica.
L'effetto si associa ad un miglioramento dell'acuità visiva, ma pare essere solo temporaneo. In casi selezionati di occlusione venosa di branca alcuni autori hanno proposto la decompressione chirurgica presso l'incrocio arterovenoso.
La presenza di una guaina avventizia comune in corrispondenza dell'incrocio arterovenoso ha un ruolo essenziale nella patogenesi dell'occlusione di branca.
Questo approccio chirurgico mira a ridurre la compressione del vaso arterioso su quello venoso favorendo il deflusso ematico.
I risultati descritti appaiono estremamente interessanti con miglioramento della velocità di flusso ematico e riduzione dell'EM.
Infatti il trattamento laser a griglia assicura un riassorbimento dell'EM senza determinare un miglioramento della funzione visiva.
La prevalenza di EM secondario ad Occlusione Venosa Retinica di Branca è stato riportata tra il 48% ed il 67%.
Inoltre lo studio multicentrico del Branch Vein Occlusion Study Group ha provato che il trattamento laser a griglia è in grado di ridurre l'EM e migliorare l'acuità visiva.
In tal modo il trattamento laser a griglia è indicato per l'EM associato ad Occlusione Venosa Retinica di Branca, ma non per l'EM associato ad Occlusione Venosa Retinica Centrale.
Sono stati pertanto proposti ed analizzati approcci terapeutici alternativi per risolvere l'EM, quali la creazione di una anastomosi corioretinica mediante laser, l'impiego di attivatore del plaminogeno tissutale, la decompressione chirurgica del nervo ottico, la vitrectomia, l'emodiluizione e l'iniezione intravitreale di triamcinolone acetonide.
La formazione di una anastomosi chorioretinica laser-indotta è stata prospettata come una possibile soluzione per by-passare il vaso venoso centrale occluso in forme di occlusione venosa retinica centrale non-ischemiche, in modo da ridurre l'ostacolo al deflusso venoso. Una anastomosi funzionalmente valida può essere ottenuta in percentuale compresa tra il 33 ed il 63% ed è associata ad un variabile recupero visivo. Sfortunatamente questo approccio è gravato da possibili complicanze, alcune delle quali molto severe, che possono verificarsi fino al 67% dei casi.
La somministrazione per via sistemica di attivatore del plasminogeno tissutale può causare gravi complicanze generali e non è stata quindi utilizzata nella comune pratica clinica.
La sua iniezione intravitreale al fine di dissolvere il trombo, evitando le complicanze sistemiche, può invece portare ad un significativo miglioramento visivo in casi selezionati. Più recentemente alcuni autori hanno tentato di applicare direttamente la molecola sul vaso venoso occluso per mezzo di una cannulazione diretta di una branca retinica, riportando interessanti risultati.
Il razionale alla base della decompressione chirurgica del nervo ottico consiste nel concetto che una riduzione della costrizione che grava sulla vena centrale retinica può favorire il deflusso venoso, permettendo una rapido riassorbimento di emorragie retiniche ed EM con miglioramento della microcircolazione retinica.
Recentemente sono stati presentati interessanti risultati ottenuti mediante la neurotomia ottica radiale, che mira ad una decompressione sclerale attraverso un approccio per via vitreale.
L'aderenza vitreo-maculare gioca un ruolo fondamentale nella complessa patogenesi dell'EM.
Alcuni tentativi di ridurre la trazione vitreale sulla macula mediante vitrectomia del polo posteriore in forme di occlusione venosa retinica centrale con EM persistente, hanno portato a risultati incoraggianti.
Il principio base dell'emodiluizione nelle occlusioni venose retiniche si fonda sull'abbassamento dell'ematocrito per ottenere una riduzione della viscosità ematica al fine di migliorare la microcircolazione e la per fusione capillare retinica.
Diverse ricerche hanno riferito positivi risultati clinici e funzionali grazie all'emodiluizione.
In particolare, è stata descritto un incremento della acuità visiva insieme ad un miglioramento sia dei parametri emodinamici (tempo arterovenoso, velocità arteriosa media) che emoreologici (viscosità del plasma, ematocrito, fibrinogeno, aggregazione eritrocitaria).
Anche l'iniezione intravitreale di triamcinolone acetonide ha portato a risultati interessanti.
Sia l'iniezione di alti (20-25 mg), che di bassi dosaggi (4 mg) sembra in grado di promuovere la risoluzione dell'EM secondario ad occlusioni venose retiniche, come dimostrato dalla riduzione dello spessore retinico mediante tomografia a coerenza ottica.
L'effetto si associa ad un miglioramento dell'acuità visiva, ma pare essere solo temporaneo. In casi selezionati di occlusione venosa di branca alcuni autori hanno proposto la decompressione chirurgica presso l'incrocio arterovenoso.
La presenza di una guaina avventizia comune in corrispondenza dell'incrocio arterovenoso ha un ruolo essenziale nella patogenesi dell'occlusione di branca.
Questo approccio chirurgico mira a ridurre la compressione del vaso arterioso su quello venoso favorendo il deflusso ematico.
I risultati descritti appaiono estremamente interessanti con miglioramento della velocità di flusso ematico e riduzione dell'EM.
Foro maculare
di Antonio P. CiardellaIl foro maculare consiste in una soluzione di continuo che si sviluppa al centro della macula.
Il danno a carico della macula causa una riduzione delle capacità visive, con l'annebbiamento e/o la distorsione delle immagini.
Caratteristicamente è interessata la porzione centrale del campo visivo, dove può essere avvertita la presenza di una macchia grigio-nera; la visione periferica, al contrario, non è compromessa.
Le cause
Una piccola percentuale si sviluppa in seguito ad un trauma.Nella maggior parte dei casi il foro è provocato invece da forze trazionali esercitate da parte del corpo vitreo sulla superficie retinica; queste forze determinano un sollevamento della macula.
Con il passare del tempo la trazione determina l'apertura del foro.
I soggetti più frequentemente colpiti sono le donne oltre i 60 anni.
Diagnosi
Con un attento esame oftalmoscopico l'oculista è in grado di diagnosticare la presenza di un foro maculare nella maggior parte dei casi. Nelle fasi iniziali, la diagnosi può essere più complessa. In ogni caso è opportuno eseguire un'OCT e, a volte, una fluoroangiografia.Prognosi
Nella maggior parte dei casi, il foro maculare, se non viene trattato, aumenta progressivamente di dimensioni e causa una riduzione sempre più marcata della visione centrale; l'acuità visiva può scendere a livelli inferiori a 1/10. Assai più raramente il foro maculare (negli stadi iniziali) può regredire.Possibilità terapeutiche
Fino a pochi anni fa il foro maculare era considerato una patologia non trattabile.L'evoluzione delle tecniche chirurgiche ha fatto sì che oggi la chiusura del foro possa essere ottenuta nella maggior parte dei casi attraverso un intervento noto come vitrectomia.
Questo può essere eseguito in anestesia locale ed in regime ambulatoriale: ciò consente al paziente di essere dimesso dal Centro dopo poche ore.
La vitrectomia porta alla rimozione delle trazioni che il vitreo esercita sulla retina e delle eventuali membrane fibrotiche che circondano il foro.
Un miglioramento della funzione visiva si verifica nella maggior parte dei casi; l'entità del miglioramento varia comunque da paziente a paziente: alcuni possono notare differenze notevoli, altri solo un modesto recupero visivo.
Fattori che influenzano la prognosi visiva sono rappresentati dalle dimensioni del foro e dalla sua durata nel tempo.
Al termine della chirurgia nell'occhio si inietta una piccola quantità di gas; questo si riassorbe in circa 2 settimane ed è gradualmente sostituito dai liquidi che fisiologicamente l'occhio produce.
Il gas serve per tamponare la retina e richiede - nei primi giorni- un posizionamento costante a faccia in giu.
Il mantenimento di tale posizione permette al gas di esercitare una pressione contro la porzione posteriore dell'occhio (dov'è situata la macula) e facilita, di conseguenza, la chiusura del foro.
 "Il foro maculare: definizione, storia, cause, evoluzione"...
"Il foro maculare: definizione, storia, cause, evoluzione"... di Antonio P. Ciardella - da Fondazione per la macula ONLUS
torna al menù
Maculopatia diabetica
di Massimo Nicolò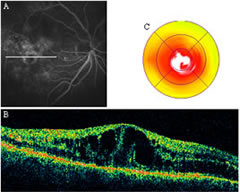 L'edema maculare è il risultato finale di una serie di eventi patologici associati ad un ampio spettro di cause.
L'edema maculare è il risultato finale di una serie di eventi patologici associati ad un ampio spettro di cause.L'edema consiste in una espansione localizzata degli spazi extracellulari e/o intracellulari della retina nell'area maculare.
La predilezione della regione maculare all'edema è la conseguenza dei deboli legami della fibre di connessione interna nello strato di Henle, che consente l'accumulo del fluido che fuoriesce dai capillari retinici perifoveali.
Contribuisce inoltre il fatto che in corrispondenza della fovea non sono presenti le cellule del Muller.
Si possono formare spazi cistoidi a disposizione radiale intorno al centro maculare, in genere apprezzabili all'esame biomicroscopico del fondo oculare.
L'edema maculare diabetico si osserva in entrambe le forme di diabete (tipo I e II) e costituisce la causa più comune di perdita della funzione visiva nei pazienti diabetici.
L'edema maculare diabetico viene solitamente classificato in due sottotipi: focale e diffuso.
L'edema maculare focale consiste in aree localizzate di ispessimento retinico collegate alla alterata permeabilità di singoli microaneurismi, capillari retinici dilatati e anomalie microvascolari intraretiniche da cui fuoriesce fluido.
Spesso queste aree di ispessimento retinico sono circondate e delimitate da essudati lipidici.
La fluorangiografia è spesso utilizzata per dimostrarne la presenza delle anomalie microvascolari e la loro anomala permeabilità. L'edema maculare diffuso è caratterizzato da una fuoriuscita generalizzata di fluido dai capillari retinici dilatati su gran parte del polo posteriore. Si associa spesso l'occlusione di una considerevole porzione del letto capillare.
L'edema maculare diffuso è di solito simmetrico nei due occhi e non si accompagna ad una significativa essudazione lipidica.
L'edema maculare diffuso è associato a diversi fattori di rischio sistemici e oculari quali: malattie renali e cardiovascolari, ipertensione sistemica grave, diabete di tipo II, numero crescente di microaneurismi, retinopatia avanzata e trazione vitreomaculare.
La percentuale di occhi con edema maculare è del 3% nei casi con retinopatia non proliferante di grado lieve, del 38% nei casi con retinopatia non proliferante di grado moderato-severo, del 71% nei casi con retinopatia proliferante.
L'edema maculare insorge più precocemente nei pazienti con diabete di tipo II.
Tra i pazienti con diabete di tipo I è inusuale l'insorgenza di edema maculare prima degli 8 anni di durata del diabete.
Esami diagnostici
L'edema maculare è la conseguenza della rottura delle barriere ematoretiniche (BER).Questa rottura può avvenire a livello dell'epitelio pigmentato retinico, ma soprattutto delle cellule endoteliali dei capillari retinici.
La fluorangiografia retinica è un esame in grado di dimostrare la distruzione della BER e di evidenziare l'edema nella sua estensione.
Una valutazione quantitativa dell'ispessimento retinico si può ottenere con la tomografia ottica a radiazione coerente (OCT), un esame non invasivo e ben tollerato.
Trattamenti
Trattamento laserL'edema maculare diabetico può migliorare dopo un trattamento laser focale o a griglia.
La maggior parte degli autori è d'accordo nel confermare che l'effetto migliore del trattamento laser si ottiene in presenza di un leakage localizzato (edema focale).
Nel caso in cui si debba procedere con la fotocoagulazione panretinica per una retinopatia proliferante, questa dovrebbe essere iniziata dopo il trattamento dell'eventuale edema maculare associato per eviterne un ulteriore peggioramento.
L'Early Treatment Diabetic Retinopathy Study (ETDRS) ha dimostrato l'utilità del trattamento laser per l'"edema maculare clinicamente significativo".
Rientrano in questa definizione i casi che presentano una o più delle seguenti caratteristiche:
- spessimento retinico entro i 500 micron centro maculare;
- essudati lipidici entro i 500 micron dal centro della macula, se associato a ispessimento della retina adiacente;
- una zona di ispessimento retinico grande una o più aree papillari, situata a meno di un diametro papillare dal centro della macula.
Il trattamento laser ha lo scopo di chiudere
i microaneurismi responsabili delle aree focali di edema retinico.
Si associa se necessario una fotocoagulazione a griglia su eventuali zone di iperpermeabilità capillare diffusa.
Iniezioni intravitreali di steroidi
L'iniezione intravitreale di triamcinolone acetonide (IVT) è stata usata di recente da sola o in unione al trattamento fotocoagulativo per l'edema maculare diabetico.
Uno studio di una serie di casi esaminati in modo prospettico e non comparativo ha rilevato che i pazienti trattati mediante IVT con una dose di 4 mg avevano un significativo miglioramento della funzione visiva a 3 mesi e 6 mesi di follow-up.
Si osservava anche una riduzione dello spessore retinico, misurato mediante OCT, durante gli stessi intervalli di follow-up.
In altri studi è stata utilizzata una dose di 20-25 mg di triamcinolone che ha portato a risultati sovrapponibili sia dal punto di vista della funzione visiva che dello spessore retinico.
Tuttavia l'effetto positivo sullo spessore retinico e sulla funzione visiva è transitorio e di solito dura circa 5-6 mesi. In diversi casi (circa il 35%) si verifica un aumento della pressione intraoculare che tuttavia viene ben compensata da un trattamento topico con farmaci ipotonizzanti e tende nel tempo a risolversi. Si può assistere anche alla progressione di una cataratta.
È bene precisare inoltre che, sebbene raramente, si possono verificare complicanze gravi quali distacco di retina, emorragie vitreali e infezioni intraoculari.
Trattamento chirurgico
Si ritiene che gli edemi maculari diabetici che non rispondono al trattamento laser possano essere conseguenza non solo di un disturbo del microcircolo ma soprattutto di una trazione meccanica che il vitreo eserciterebbe sulla retina maculare.
Diversi studi clinici sembrano suggerire che la vitrectomia potrebbe avere un effetto benefico in questo edema maculare diabetico di tipo trazionale.
L'OCT è l'esame più importante per riconoscere queste forme.
Sulla base di dati pubblicati, dal 38% al 100% dei pazienti sottoposti a vitrectomia per edema maculare diabetico trazionale mostravano un miglioramento della funzione visiva.
Anche in questo caso si tratta di studi non randomizzati, non controllati e retrospettivi, con un numero esiguo di pazienti.
Iniezioni intravitreali di steroidi
L'iniezione intravitreale di triamcinolone acetonide (IVT) è stata usata di recente da sola o in unione al trattamento fotocoagulativo per l'edema maculare diabetico.
Uno studio di una serie di casi esaminati in modo prospettico e non comparativo ha rilevato che i pazienti trattati mediante IVT con una dose di 4 mg avevano un significativo miglioramento della funzione visiva a 3 mesi e 6 mesi di follow-up.
Si osservava anche una riduzione dello spessore retinico, misurato mediante OCT, durante gli stessi intervalli di follow-up.
In altri studi è stata utilizzata una dose di 20-25 mg di triamcinolone che ha portato a risultati sovrapponibili sia dal punto di vista della funzione visiva che dello spessore retinico.
Tuttavia l'effetto positivo sullo spessore retinico e sulla funzione visiva è transitorio e di solito dura circa 5-6 mesi. In diversi casi (circa il 35%) si verifica un aumento della pressione intraoculare che tuttavia viene ben compensata da un trattamento topico con farmaci ipotonizzanti e tende nel tempo a risolversi. Si può assistere anche alla progressione di una cataratta.
È bene precisare inoltre che, sebbene raramente, si possono verificare complicanze gravi quali distacco di retina, emorragie vitreali e infezioni intraoculari.
Trattamento chirurgico
Si ritiene che gli edemi maculari diabetici che non rispondono al trattamento laser possano essere conseguenza non solo di un disturbo del microcircolo ma soprattutto di una trazione meccanica che il vitreo eserciterebbe sulla retina maculare.
Diversi studi clinici sembrano suggerire che la vitrectomia potrebbe avere un effetto benefico in questo edema maculare diabetico di tipo trazionale.
L'OCT è l'esame più importante per riconoscere queste forme.
Sulla base di dati pubblicati, dal 38% al 100% dei pazienti sottoposti a vitrectomia per edema maculare diabetico trazionale mostravano un miglioramento della funzione visiva.
Anche in questo caso si tratta di studi non randomizzati, non controllati e retrospettivi, con un numero esiguo di pazienti.
torna al menù
Maculopatia miopica
di Luca VentreLa miopia patologica o degenerativa è caratterizzata da alterazioni anatomo-cliniche dovute all'eccessivo allungamento del bulbo oculare con conseguenti alterazioni del polo posteriore e della periferia retinica.
In questi casi il difetto rifrattivo è superiore alle 6 diottrie e la lunghezza assiale del bulbo supera i 26 mm.
La prevalenza della miopia varia dall'11 al 36%, a seconda delle casistiche, con differenze etniche (più frequente nelle popolazioni asiatiche) e di sesso (con un rapporto maschi/femmine di 1/2).
La prevalenza della miopia patologica varia tra lo 0.2% e il 9.6%.
L'importanza di questa patologia risiede nel fatto che è un'importante causa di minorazione visiva in pazienti giovani (età inferiore ai 50 anni).
Negli USA è la settima causa di cecità legale dopo i 20 anni di età, in Giappone ed in Europa la quinta.
Le alterazioni che possono interessare il polo posteriore sono essenzialmente di due tipi: distrofiche(stafiloma miopico, rotture della membrana di Bruch, atrofia corioretinica, tilted disc syndrome, schisi retinica al polo posteriore, distacco di retina posteriore) ed essudative (neovascolarizzazione coroideale).
Stafiloma miopico
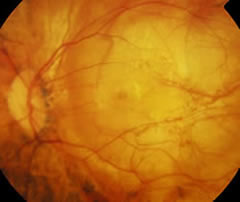 È uno sfiancamento del bulbo oculare, accompagnato da una serie di alterazioni degenerative della coroide e della
retina.
È uno sfiancamento del bulbo oculare, accompagnato da una serie di alterazioni degenerative della coroide e della
retina.Nel 50% dei casi è localizzato al polo posteriore, ma può avere sede peripapillare, nasale (configurando il quadro detto "miopia inversa") o inferiore (e configura la "Tilted disk syndrome", vedi dopo).
Lo stafiloma è presente già in età giovanile e aumenta con l'età.
All'esame biomicroscopico appare come un'area pallida e attraverso la quale si intravedono i vasi coroideali profondi.
Talvolta sono presenti alterazioni dell'epitelio pigmentato retinico (EPR) ai bordi dello stafiloma.
La sede dello stafiloma è molto importante per la prognosi visiva: oltre il 50% degli occhi con stafiloma centrale è legalmente cieco dopo i 60 anni di età.
Distrofia e atrofia corioretinica
La retina, in corrispondenza dello stafiloma, presenta vasi stirati e la macula lutea diventa spesso indistinguibile.
L'assottigliamento dell'EPR e della coriocapillare determinano una maggiore evidenza della trama vascolare coroideale.
Spesso queste aree di assottigliamento evolvono verso la completa atrofia corioretinica ed appaiono come isole giallastre, in cui si vede direttamente la sclera, attraversate da rari, grossi vasi coroideali.
L'assottigliamento dell'EPR e della coriocapillare determinano una maggiore evidenza della trama vascolare coroideale.
Spesso queste aree di assottigliamento evolvono verso la completa atrofia corioretinica ed appaiono come isole giallastre, in cui si vede direttamente la sclera, attraversate da rari, grossi vasi coroideali.
Tilted disc syndrome
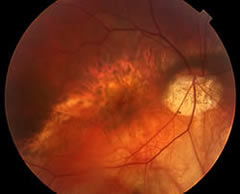 È caratterizzata dalla presenza di uno stafiloma decentrato, di solito, in sede infero-nasale, con i bordi che attraversano
l'area maculare.
È caratterizzata dalla presenza di uno stafiloma decentrato, di solito, in sede infero-nasale, con i bordi che attraversano
l'area maculare.Il grado di miopia può essere anche minore alle 6 diottrie, ma in genere è presente un astigmatismo di 2 o 3 diottrie dovuto all'irregolarità del polo posteriore.
La papilla ottica presenta una forma ovale a maggior asse orizzontale ed è circondata da un'area di atrofia corioretinica nei settori inferiori.
Nella regione maculare è spesso presente una distrofia dell'EPR che coincide con il margine dello stafiloma.
In quest'area si possono sviluppare delle neovascolarizzazioni coroideali (CNV) subfoveali o juxtafoveali.
Rotture della membrana di Bruch
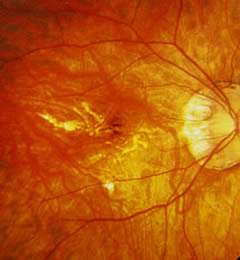 Sono presenti in circa il 4% degli occhi con una lunghezza assiale superiore ai 26.5 mm, ma il loro numero e la loro
estensione non sono correlati direttamente alla lunghezza assiale.
Sono presenti in circa il 4% degli occhi con una lunghezza assiale superiore ai 26.5 mm, ma il loro numero e la loro
estensione non sono correlati direttamente alla lunghezza assiale.La loro presenza in corrispondenza della fovea è causa di deterioramento visivo centrale.
Spesso sono causa di emorragie maculari sottoretiniche improvvise, in assenza di CNV.
In questi casi la prognosi visiva è favorevole, purché la rottura della membrana di Bruch non abbia coinvolto la fovea.
All'esame oftalmoscopico appaiono come linee giallastre di calibro irregolare, a decorso orizzontale, singole o multiple.
L'esame fluorangiografico può aiutare a metterle in evidenza, soprattutto quando sono sottili e sfuggono all'esame oftalmoscopico. Appaiono come linee iperfluorescenti senza diffusione del colorante.
All'angiografia con ICG appaiono invece come linee ipofluorescenti.
Distacco della retina
Il distacco di retina posteriore origina da un foro
maculare e rimane generalmente confinato entro le arcate vascolari.
Con il passare del tempo si può osservare una degenerazione cistoide della retina sollevata.
L'introduzione dell'esame OCT ha permesso di studiare in modo più dettagliato le caratteristiche dei sollevamenti retinici al polo posteriore nella miopia patologica.
Accanto al classico sollevamento retinico al polo posteriore determinato dal foro maculare si può osservare nel miope una schisi retinica posteriore, accompagnata o meno da un foro maculare.
La sintomatologia di tali sollevamenti può essere lieve, la terapia è solo chirurgica, ma è controversa la scelta di intervenire, in quanto la lesione ha una scarsa evolutività e il recupero funzionale dopo la chirurgia è modesto.
Con il passare del tempo si può osservare una degenerazione cistoide della retina sollevata.
L'introduzione dell'esame OCT ha permesso di studiare in modo più dettagliato le caratteristiche dei sollevamenti retinici al polo posteriore nella miopia patologica.
Accanto al classico sollevamento retinico al polo posteriore determinato dal foro maculare si può osservare nel miope una schisi retinica posteriore, accompagnata o meno da un foro maculare.
La sintomatologia di tali sollevamenti può essere lieve, la terapia è solo chirurgica, ma è controversa la scelta di intervenire, in quanto la lesione ha una scarsa evolutività e il recupero funzionale dopo la chirurgia è modesto.
Neovascolarizzazione coroideale
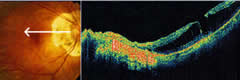 È una delle complicanze più temibili per la prognosi visiva nella
miopia patologica.
È una delle complicanze più temibili per la prognosi visiva nella
miopia patologica.Colpisce il 5 - 10% degli occhi affetti da miopia patologica.
Circa 1/3 delle CNV compare in corrispondenza di una rottura della membrane di Bruch. Clinicamente si manifesta con visione distorta e annebbiata o scotoma assoluto centrale in presenza di emorragie sottoretiniche.
Oftalmoscopicamente si rileva in genere una lieve essudazione retinica accompagnata da piccole emorragiole retiniche. La CNV si apprezza come una lesione grigiastra di piccole dimensioni e forma tondeggiante.
All'esame fluorangiografico la CNV appare come un'area tondeggiante, iperfluorescente, con tendenza a diffusione del colorante nelle fasi tardive.
Si trova in sede subfoveale nel 65% dei casi; nei restanti casi è localizzata entro 100-300 µm dalla fovea.
La dimensione iniziale della CNV è quasi sempre inferiore a metà area papillare.
Talvolta risulta difficoltoso individuarla a causa del mascheramento da parte di una emorragia retinica oppure perché l'iperfluorescenza della lesione si confonde con quella di un'area di atrofia corioretinica adiacente o di una rottura della membrana di Bruch.
In questi casi può essere dirimente l'angiografia con verde di indocianina in quanto la radiazione infrarossa utilizzata in questo esame supera bene le emorragie retiniche; inoltre le aree di atrofia corioretinica e le rotture della membrana di Bruch sono ipofluorescenti in contrasto con la CNV.
Con il passare del tempo la membrana neovascolare diventa iperpigmentata e costituisce la lesione nota come macchia di Fuchs, che viene progressivamente sostituita da un'area di atrofia corioretinica coinvolgente più meno il polo posteriore.
La fotocoagulazione laser è stata per lungo tempo l'unica terapia per la CNV miopica extrafoveale.
I principali inconvenienti di questa terapia sono:
- L'alta percentuale di recidive, sempre sul lato foveale della cicatrice (circa il 50% di recidiva, la maggior parte entro il primo anno di follow-up);
- L'estensione sul versante foveale della cicatrice creata dal laser.
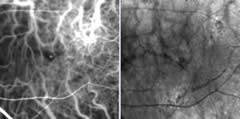 L'avvento della terapia fotodinamica (PDT) ha cambiato l'approccio terapeutico della CNV miopica.
L'avvento della terapia fotodinamica (PDT) ha cambiato l'approccio terapeutico della CNV miopica.Questa terapia è più selettiva e risparmia il tessuto retinico sovrastante la lesione. Sono diventate trattabili quindi anche le CNV centrali subfoveali.
Lo studio VIP (Verteporfin In Photodynamic therapy) ha dimostrato l'utilità della PDT per il trattamento della CNV subfoveale della miopia patologica. Sono spesso necessari due o più trattamenti, a causa della riattivazione della CNV.
I vantaggi rispetto alla fotocoagulazione con laser termico possono far optare per la PDT anche in caso di neovascolarizzazioni extrafoveale.
Non vi sono ancora dati significativi sulla validità di un approccio chirurgico volto ad asportare la membrana neovascolare sottoretinica.
torna al menù
Maculopatia Senile: niente vitamine
da British Medical JournalUna delle malattie oculari di cui si parla più frequentemente negli ultimi tempi è la degenerazione maculare senile o degenerazione maculare correlate all'età.
Ai pazienti oculistici è comunemente più nota come maculopatia senile.
Questa malattia, come dice il nome, colpisce la macula della retina cioè la parte centrale e più nobile della retina: quella che ci permette di vedere i minimi particolari.
Per esempio è la macula che ci permette di vedere le dieci righe dell'ottotipo, cioè del tabellone con le lettere che l'oculista fa leggere al paziente per definire la sua acuità visiva e le eventuali lenti di cui ha bisogno.
Se questa zona della retina è malata si può arrivare alla cecità legale, cioè non vedere nemmeno la riga del tabellone corrispondente a 1/10 su 10/10 a metà della distanza standard regolare.
Negli ultimi anni si sono ampliate le possibilità diagnostiche: prima esisteva solo la angiografia retinica con fluoresceina o fluorangiografia,adesso esiste anche la angiografia con verde di indocianina e l'OCT o tomografia ottica a coerenza.
Queste strumentazioni permettono di distinguere le forme di maculopatia che possono avere dei benefici da terapie mediche, parachirurgiche, chirurgiche.
In effetti anche le possibilità terapeutiche sono aumentate: un tempo c'era solo il trattamento con argon laser, che inevitabilmente danneggiava anche le parti sane del tessuti trattato, adesso esiste la terapia fotodinamica che è selettiva andando a colpire solo le parti malate e le iniezioni endoculari con cortisone o sostanze di tipo anti-tumorale.
Tutte queste terapie però nel complesso servono per bloccare la patologia o per rallentarla, difficilmente portano ad un miglioramento.
Si è pensato quindi anche alla prevenzione. Essa si basa sull'evitare i fattori che possono favorire la comparsa della maculopatia: raggi solari, fumo e tutti i fattori che influiscono negativamente sulla circolazione come ad es. il diabete mellito. Negli ultimi anni sono stati proposti farmaci o, per meglio dire, integratori a base di vitamine, antiossidanti ed altri prodotti "protettivi".
Una revisione di tutti i principali studi inerenti l'uso di vitamina A, vitamina C, vitamina E, zinco, luteina, alfa e beta carotene nella prevenzione della maculopatia senile ha portato ad una metanalisi, cioè ad una analisi statistica di tutti i dati nel loro insieme.
Da ciò è risultato che non c'è una riduzione del rischio di essere colpiti da una maculopatia senile con l'assunzione di questi prodotti.
(Da British Medical Journal)
Tomografia a coerenza ottica
di Roberta Rigault de la LongraisLa tomografia a coerenza ottica, o OCT (Optical Coherence Tomography), è una recente tecnica di imaging, non invasiva, che fornisce immagini ad alta risoluzione di sezioni della retina umana in vivo, permettendo la diagnosi, la stadiazione ed il follow-up di numerose affezioni retiniche.
Il potere di risoluzione longitudinale dell'OCT di nuova generazione (OCT III) è di circa 7-10 µm, ben superiore a quello di altre tecniche di diagnosi per immagine, come l'ecografia B-scan e l'oftalmoscopia a scansione laser, che forniscono rispettivamente immagini con una risoluzione di 150 e 300 µm.
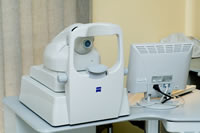 L'OCT funziona tramite una tecnica di misurazione ottica chiamata interferometria a bassa coerenza.
L'OCT funziona tramite una tecnica di misurazione ottica chiamata interferometria a bassa coerenza.Il principio di funzionamento dell'interferometria è simile a quello dell'ecografia, differenziandosene per il fatto di sfruttare la riflessione di onde luminose da parte delle diverse strutture oculari piuttosto che la riflessione delle onde acustiche.
La caratteristica principale consiste nel fatto che la velocità della luce è quasi un milione di volte più veloce di quella del suono, consentendo la misurazione di strutture e distanze dell'ordine di 10 µm, contro i 100-150 degli ultrasuoni.
Un'altra caratteristica importante è che l'interferometria ottica, a differenza degli ultrasuoni, non richiede alcun contatto fisico con il tessuto esaminato.
L'OCT proietta sulla retina un fascio di lunghezza d'onda nel vicino infrarosso (820 nm) generato da un diodo superluminescente; confronta quindi i tempi di propagazione dell'eco della luce riflessa dalla retina con quelli relativi allo stesso fascio di luce riflesso da uno specchio di riferimento posto a distanza nota.
Benché la luce riflessa dalla retina sia composta da eco multipli, la distanza percorsa dagli stessi viene determinata tramite la variazione della distanza dallo specchio di riferimento.
L'interferometro OCT rileva elettronicamente, raccoglie, elabora e memorizza gli schemi di ritardo dell'eco provenienti dalla retina.
I tomogrammi vengono visualizzati in tempo reale utilizzando una scala in falsi colori che rappresenta il grado di reflettività dei tessuti posti a diversa profondità: i colori scuri (blu e nero) rappresentano zone a minima reflettività ottica, mentre i colori chiari come il rosso ed il bianco definiscono zone molto riflettenti.
Infine il sistema memorizza le scansioni selezionate, permettendone la successiva elaborazione, tra cui la possibilità di correggere l'effetto dei movimenti oculari longitudinali (ma non di quelli trasversali).
L'OCT è quindi un esame semplice, rapido, non invasivo ed altamente riproducibile, ma è limitato dalla presenza di qualsiasi opacità dei mezzi diottrici (edema o leucomi corneali, cataratta, emovitreo) e dalla miosi.
Le immagini tomografiche ottenute con l'OCT permettono uno studio sia di tipo qualitativo che quantitativo del tessuto retinico, con la possibilità di dirigere la scannerizzazione direttamente verso la zona di interesse grazie alla contemporanea osservazione della retina.
Dal punto di vista qualitativo su ogni scansione si può effettuare un'analisi della morfologia e del grado di reflettività degli strati retinici.
Per quanto riguarda la valutazione quantitativa lo strumento permette di misurare lo spessore della retina, che può anche essere rappresentato in mappe di spessore.
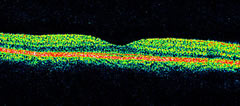 Nella sezione tomografica della regione maculare in condizioni normali si visualizza la caratteristica struttura retinica a
strati con la depressione foveale. La superficie di separazione vitreo-retinica appare ben definita, grazie al contrasto tra
l'assenza di reflettività del vitreo e la alevata reflettività dello strato delle fibre nervose più superficiali.
Nella sezione tomografica della regione maculare in condizioni normali si visualizza la caratteristica struttura retinica a
strati con la depressione foveale. La superficie di separazione vitreo-retinica appare ben definita, grazie al contrasto tra
l'assenza di reflettività del vitreo e la alevata reflettività dello strato delle fibre nervose più superficiali.Gli strati retinici intermedi possiedono un modesto grado di reflettività.
I fotorecettori, che hanno una disposizione longitudinale, sono otticamente poco riflettenti ed appaiono come una banda scura che separa la neuroretina dal complesso epitelio pigmentato-coriocapillare di elevata reflettività.
Qualche debole segnale di reflettività proviene anche dagli strati più profondi della coroide e della sclera, soprattutto nei casi di assottigliamento o atrofia del tessuto retinico.
Membrane epiretiniche a foro maculare
Attualmente l'OCT è considerato un esame strumentale complementare alla fluoroangiografia ed alla fotografia del fondo oculare per lo studio delle patologie retiniche, ma si sta sempre più sostituendo ad essi soprattutto per quanto riguarda la stadiazione ed il follow-up delle alterazioni dell'interfaccia vitreo-retinica e dei fori maculari.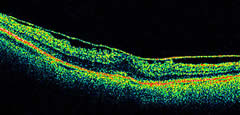 Nelle fibrosi pre-retiniche (pucker maculare) l'OCT evidenzia un
aumento di reflettività della membrana limitante interna o la chiara presenza di una membrana epiretinica, sotto forma di una
banda più o meno spessa, di tessuto iperriflettente adeso in uno o più punti alla superficie retinica.
Nelle fibrosi pre-retiniche (pucker maculare) l'OCT evidenzia un
aumento di reflettività della membrana limitante interna o la chiara presenza di una membrana epiretinica, sotto forma di una
banda più o meno spessa, di tessuto iperriflettente adeso in uno o più punti alla superficie retinica.Le trazioni di tali membrane sulla retina vengono chiaramente documentate.
Si possono osservare aumento dello spessore retinico, scomparsa della depressione foveale e presenza di aree a diminuita reflettività all'interno della retina, indice di edema intraretinico.
L'OCT si è rivelato di grande utilità diagnostica e soprattutto prognostica nel caso dei fori maculari, aiutando a riconoscerne
i diversi stadi evolutivi.
L'OCT di un foro maculare allo stadio IV mostra una perdita di sostanza a tutto spessore, con bordi ispessiti per edema intraretinico, arrotondati e parzialmente sollevati da liquido sottoretinico.
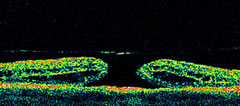 L'OCT risulta inoltre di grande utilità per la diagnosi differenziale con
il foro maculare lamellare, non a tutto spessore,
dimostrando con precisione istologica come in quest'ultimo caso la perdita di sostanza interessi solo una parte degli strati
retinici interni.
L'OCT risulta inoltre di grande utilità per la diagnosi differenziale con
il foro maculare lamellare, non a tutto spessore,
dimostrando con precisione istologica come in quest'ultimo caso la perdita di sostanza interessi solo una parte degli strati
retinici interni.
L'OCT è quindi l'esame più indicato per selezionare i casi di foro maculare e di sindrome dell'interfaccia vitreo-retinica potenzialmente suscettibili di trattamento chirurgico (vitrectomia).
La possibilità di misurare le dimensioni del foro maculare assume una notevole importanza a fini prognostici nella programmazione dell'intervento.
L'OCT di un foro maculare allo stadio IV mostra una perdita di sostanza a tutto spessore, con bordi ispessiti per edema intraretinico, arrotondati e parzialmente sollevati da liquido sottoretinico.
 L'OCT risulta inoltre di grande utilità per la diagnosi differenziale con
il foro maculare lamellare, non a tutto spessore,
dimostrando con precisione istologica come in quest'ultimo caso la perdita di sostanza interessi solo una parte degli strati
retinici interni.
L'OCT risulta inoltre di grande utilità per la diagnosi differenziale con
il foro maculare lamellare, non a tutto spessore,
dimostrando con precisione istologica come in quest'ultimo caso la perdita di sostanza interessi solo una parte degli strati
retinici interni.L'OCT è quindi l'esame più indicato per selezionare i casi di foro maculare e di sindrome dell'interfaccia vitreo-retinica potenzialmente suscettibili di trattamento chirurgico (vitrectomia).
La possibilità di misurare le dimensioni del foro maculare assume una notevole importanza a fini prognostici nella programmazione dell'intervento.
Edema maculare
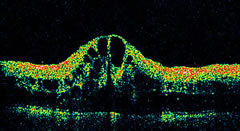 L'OCT consente una semplice e sensibile diagnosi dell'edema maculare secondario a
retinopatia diabetica, occlusione della
vena centrale della retina, uveite, fibrosi pre-retinica o
post-intervento di cataratta.
L'OCT consente una semplice e sensibile diagnosi dell'edema maculare secondario a
retinopatia diabetica, occlusione della
vena centrale della retina, uveite, fibrosi pre-retinica o
post-intervento di cataratta.In questi casi le sezioni tomografiche mostrano un aumento più o meno marcato dello spessore della retina, che può mostrare al suo interno aree tondeggianti a ridotta reflettività, segno di accumulo intraretinico di liquido (edema cistoide).
L'ispessimento retinico può essere quantificato e venir rappresentato in mappe di spessore retinico, di evidente utilità nel corso del follow-up del paziente.
L'OCT si è dimostrato molto più sensibile dell'osservazione biomicroscopica nel rilevare piccole variazioni dello
spessore retinico. Aggiunge informazioni quantitative alla classica valutazione fluorangiografica.
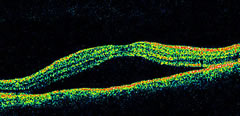 Nella CSC di tipo acuto l'OCT permette di valutare in modo oggettivo e quantificabile il distacco del neuroepitelio e
l'eventuale presenza di piccoli distacchi dell'epitelio pigmentato associati, con la possibilità di monitorarne
l'evoluzione spontanea o successiva a trattamento fotocoagulativo.
Nella CSC di tipo acuto l'OCT permette di valutare in modo oggettivo e quantificabile il distacco del neuroepitelio e
l'eventuale presenza di piccoli distacchi dell'epitelio pigmentato associati, con la possibilità di monitorarne
l'evoluzione spontanea o successiva a trattamento fotocoagulativo.
Anche piccoli sollevamenti del neuroepitelio, non clinicamente identificabili all'esame biomicroscopico, possono essere evidenziati dall'OCT sotto forma di sottili bande a ridotta reflettività comprese tra il complesso EPR-coriocapillare e lo strato dei fotorecettori.
Nei casi di CSC cronica l'OCT fa rilevare alterazioni degenerative a livello dei fotorecettori fino alla loro atrofia, e può dare informazioni sulla prognosi funzionale. In alcuni casi avanzati si rileva una degenerazione cistoide del tessuto retinico maculare.
Corioretinopatia sierosa centrale (CSC)
 Nella CSC di tipo acuto l'OCT permette di valutare in modo oggettivo e quantificabile il distacco del neuroepitelio e
l'eventuale presenza di piccoli distacchi dell'epitelio pigmentato associati, con la possibilità di monitorarne
l'evoluzione spontanea o successiva a trattamento fotocoagulativo.
Nella CSC di tipo acuto l'OCT permette di valutare in modo oggettivo e quantificabile il distacco del neuroepitelio e
l'eventuale presenza di piccoli distacchi dell'epitelio pigmentato associati, con la possibilità di monitorarne
l'evoluzione spontanea o successiva a trattamento fotocoagulativo.Anche piccoli sollevamenti del neuroepitelio, non clinicamente identificabili all'esame biomicroscopico, possono essere evidenziati dall'OCT sotto forma di sottili bande a ridotta reflettività comprese tra il complesso EPR-coriocapillare e lo strato dei fotorecettori.
Nei casi di CSC cronica l'OCT fa rilevare alterazioni degenerative a livello dei fotorecettori fino alla loro atrofia, e può dare informazioni sulla prognosi funzionale. In alcuni casi avanzati si rileva una degenerazione cistoide del tessuto retinico maculare.
Degenerazione maculare legata all'età (AMD)
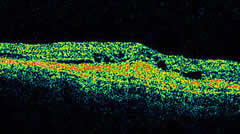 Nell'AMD essudativa l'OCT può essere associato agli esami angiografici
per avere ulteriori informazioni sulle caratteristiche strutturali della membrana neovascolare, sulla sua
localizzazione al di sopra o al di sotto daell'epitelio pigmentato retinico e sulla presenza di attività essudativa
intra e sottoretinica.
Nell'AMD essudativa l'OCT può essere associato agli esami angiografici
per avere ulteriori informazioni sulle caratteristiche strutturali della membrana neovascolare, sulla sua
localizzazione al di sopra o al di sotto daell'epitelio pigmentato retinico e sulla presenza di attività essudativa
intra e sottoretinica.L'OCT fa rilevare eventuali distacchi dell'epitelio pigmentato associati alla neovascolarizzazione.
L'OCT può essere particolarmente utile nel follow-up dopo terapia fotodinamica per confermare o meno l'attività essudativa di una lesione quando la fluorangiografia lascia dubbi, e per porre quindi le indicazioni ad un ritrattamento.
L'OCT può essere anche utile per riconoscere e studiare strutturalmente forme particolari di neovascolarizzazione come la vasulopatia coroideale polipoide e la RAP (proliferazione angiomatos retinica).
torna al menù
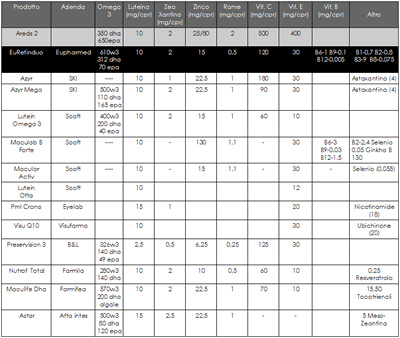
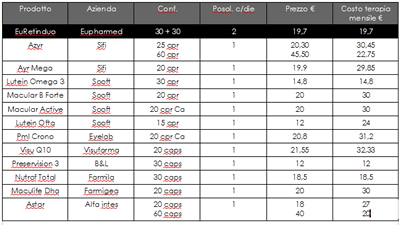
Terapie possibili e disponibili sul mercato
Tabella di tutti i farmaci a disposizione per la terapia delle maculopatie delle varie case farmaceutiche, con
la percentuale dei dosaggi e dei vari componenti farmacologici rispetto allo studio AREDS 2 sulla terapia delle
maculopatie.