la sindrome dell'occhio secco
La sindrome dell'occhio secco : cause e caure
A cura della D.ssa Maria Angela Molinaro
Definizione e cause
 L'occhio secco è una malattia di frequente osservazione, con una incidenza aumentata significativamente negli ultimi anni,
purtroppo spesso sottovalutata o non diagnosticata ad una prima osservazione clinica.
L'occhio secco è una malattia di frequente osservazione, con una incidenza aumentata significativamente negli ultimi anni,
purtroppo spesso sottovalutata o non diagnosticata ad una prima osservazione clinica. Con il termine "sindrome da occhio secco " si indica generalmente l'alterazione quantitativa o qualitativa delle lacrime che inumidiscono la superficie oculare a contatto con l'esterno.
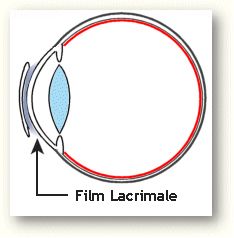
In realtà, è dalla concomitanza di molti più fattori che origina una secchezza oculare, in quanto il film lacrimale pre-oculare ed i tessuti corneale e congiuntivale funzionano in mutua interrelazione.
Molte sono le definizioni di occhio secco; quella riconosciuta dalla comunità scientifica internazionale è che: l'occhio secco è una patologia del film lacrimale dovuta a ridotta produzione o eccessiva evaporazione delle lacrime, che procura danno alla superficie oculare interpalpebrale esposta ed è associata a sintomi di discomfort.
Le lacrime hanno una particolare composizione ed una modalità di secrezione, tali da poter compiere quattro funzioni
- lubrificare la cornea;
- contribuire al potere refrattivo dell'occhio, costituendo la superficie di contatto tra cornea e aria;
- nutrire la cornea;
- svolgere una azione antibatterica.
La loro produzione normale è di 0.8 microlitri/minuto circa.
Il film lacrimale è mantenuto qualitativamente e quantitativamente costante, grazie all'azione combinata della secrezione (ghiandole secretorie), dalla distribuzione per ammiccamento palpebrale e dalla escrezione che avviene attraverso le ghiandole lacrimali.
Il film lacrimale è prodotto da numerose ghiandole :
Il film lacrimale è mantenuto qualitativamente e quantitativamente costante, grazie all'azione combinata della secrezione (ghiandole secretorie), dalla distribuzione per ammiccamento palpebrale e dalla escrezione che avviene attraverso le ghiandole lacrimali.
Il film lacrimale è prodotto da numerose ghiandole :
- dalle ghiandole che stanno sul bordo palpebrale,
- dalla ghiandola lacrimale,
- da cellule secernenti isolate e sparse nella congiuntiva.
Tutte queste ghiandole non producono lo stesso secreto, tanto è vero che il film lacrimale è costituito da tre strati
principali, ognuno dei quali risulta essere fondamentale affinché il film stesso possa svolgere la propria funzione.
La parte principale del film lacrimale è costituita da acqua che contiene sali, zuccheri, proteine, enzimi e altre sostanze.
Questo strato è capace di portare le sostanze nutritive e di difesa alla cornea e alla congiuntiva, le quali riversano in esso i prodotti del loro metabolismo sia in situazioni fisiologiche che patologiche.
Per evitare l'evaporazione dell'acqua, lo strato più esterno è costituito da uno strato lipidico che ha il compito di mantenere uniforme lo spessore del film lacrimale, inoltre garantisce la levigatezza del film lacrimale.
Ogni piccola modificazione della propria viscosità o del proprio spessore determinerebbe qualche problema sulla distribuzione del film lacrimale.
Infine per mantenere l'acqua attaccata alle cellule della cornea e della congiuntiva, queste producono una sostanza particolare con la funzione di mantenere bagnabile la superficie stessa.
La parte principale del film lacrimale è costituita da acqua che contiene sali, zuccheri, proteine, enzimi e altre sostanze.
Questo strato è capace di portare le sostanze nutritive e di difesa alla cornea e alla congiuntiva, le quali riversano in esso i prodotti del loro metabolismo sia in situazioni fisiologiche che patologiche.
Per evitare l'evaporazione dell'acqua, lo strato più esterno è costituito da uno strato lipidico che ha il compito di mantenere uniforme lo spessore del film lacrimale, inoltre garantisce la levigatezza del film lacrimale.
Ogni piccola modificazione della propria viscosità o del proprio spessore determinerebbe qualche problema sulla distribuzione del film lacrimale.
Infine per mantenere l'acqua attaccata alle cellule della cornea e della congiuntiva, queste producono una sostanza particolare con la funzione di mantenere bagnabile la superficie stessa.
È necessario distinguere due forme di Sindrome da occhio secco:
- Primarie (Sindrome di Sjögren), cioè manifestazioni oculari di una malattia generale autoimmune, come ad esempio lupus eritematoso sistemico, artrite reumatoide, sclerodermia ecc.
- Secondarie, dovute ad un'eccessiva vaporizzazione del film lacrimale (blefariti, congiuntiviti, uso protratto di lenti a contatto, ridotta secrezione senile, ridotta secrezione dovuta a farmaci, a ipovitaminosi A, a uso protratto di colliri)o ad una ridotta produzione di fluido lacrimale.
Sintomatologia dell'occhio secco
I sintomi più comuni dovuti alla sindrome da occhio secco sono bruciore, sensazione di corpo estraneo nell'occhio, fotofobia,
difficoltà nell'apertura della palpebra al risveglio e, nei casi più gravi, dolore e annebbiamento visivo.
Tutti questi disturbi aumentano in ambienti secchi, ventosi o dove sono in funzione impianti di riscaldamento o di condizionamento. Talvolta, i pazienti affetti da ipolacrimia lacrimano copiosamente (soprattutto in presenza di cheratite, danno alla superficie corneale): il liquido lacrimale è però molto acquoso, contiene poche componenti mucose ed evapora velocemente lasciando la cornea esposta all'azione di agenti esterni. Molte persone affette da sindrome degli occhi secchi soffrono anche di disturbi alla gola e al seno paranasale: congestione nasale o sinusite, tosse cronica, raffreddori frequenti, allergie stagionali, congestione al centro dell'orecchio, mal di testa.
Tutti questi disturbi aumentano in ambienti secchi, ventosi o dove sono in funzione impianti di riscaldamento o di condizionamento. Talvolta, i pazienti affetti da ipolacrimia lacrimano copiosamente (soprattutto in presenza di cheratite, danno alla superficie corneale): il liquido lacrimale è però molto acquoso, contiene poche componenti mucose ed evapora velocemente lasciando la cornea esposta all'azione di agenti esterni. Molte persone affette da sindrome degli occhi secchi soffrono anche di disturbi alla gola e al seno paranasale: congestione nasale o sinusite, tosse cronica, raffreddori frequenti, allergie stagionali, congestione al centro dell'orecchio, mal di testa.
Test Clinici Diagnostici
In presenza di un paziente con occhio secco, oltre ai normali test di routine per una visita oculistica ci sono attualmente
parecchi metodi per valutare l'adeguata produzione di lacrime, questi sono:
- la misurazione del menisco lacrimale tra il bulbo ed il margine della palpebra inferiore
- il test di Schirmer (per la valutazione della produzione lacrimale)
- la colorazione con fluoresceina, rosa bengale e verde di Lisammina (che mettono in evidenza le cellule sofferenti)
- il tempo di rottura del film lacrimale (per valutare la qualità delle lacrime)
- la sensibilità al contrasto
- la citologia ad impressione per la valutazione delle cellule della congiuntiva
- l'analisi dei film lacrimale per valutare l'osmolarità, la presenza di lisozima
- il test di felcizzazione delle lacrime
- il test della clearance della fluoresceina.
Terapie Cura dell'occhio secco
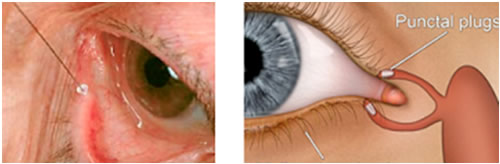 La terapia meccanica più semplice e più usata nel trattamento delle sindromi da occhio secco consiste nella chiusura,
provvisoria o definitiva, dei puntini lacrimali inferiore e/o superiore, per mezzo di piccoli tappi di silicone.
La terapia meccanica più semplice e più usata nel trattamento delle sindromi da occhio secco consiste nella chiusura,
provvisoria o definitiva, dei puntini lacrimali inferiore e/o superiore, per mezzo di piccoli tappi di silicone. L'occlusione provvisoria con tappi di acido ialuronico è consigliabile per verificare se l'ostruzione delle vie di deflusso può essere in qualche modo utile per ridurre la sintomatologia del paziente (i tamponi inseriti nei condotti di scarico lacrimali si di dissolvono in 4-7 giorni); se tale rimedio si dimostra efficace, permettendo una migliore lubrificazione dell'occhio, si ricorre alla chiusura definitiva mediante l'uso di "punctum plugs".
Disponibili in versione collagene rapido assorbimento, riassorbibile lunga permanenza, silicone permanente o nella nuova versione Hydrogel e prodotti in differenti diametri per consentire un perfetto adattamento al canale, i Punctum Plug rappresentano un'efficace risposta al problema della sindrome dell'occhio secco.
Facili da applicare ed eventualmente da rimuovere, i Punctum Plug trovano oggi sempre più frequentemente impiego nei soggetti con sindrome sicca; un apposito set di due calibri consente, con rapidità e precisione, di misurare il canale del paziente per poter determinare il diametro dei Punctum Plug più indicato.
La gamma dei "punctum plug" è composta da:
- Soft Plug collagene a rapido assorbimento (fino a 4 giorni circa)
- Soft Plug riassorbibili lunga permanenza (fino a 90 giorni circa)
- Soft Plug Form Fit Hydrogel a lunga permanenza
- Soft Plug silicone permanenti premontati
I nuovi Soft Plug in Hydrogel si inseriscono facilmente, grazie allo speciale inseritore, e in circa dieci minuti si
espandono fino a perfettamente adattarsi al diametro del punctum.
Trattamento dell'occhio secco
A tutt'oggi non esiste una terapia risolutiva della patologia da occhio secco. Nonostante esistano numerosi presidi terapeutici
topici a disposizione (in Italia esistono in commercio circa 120 sostituti lacrimali), i risultati a lungo termine della
terapia delle affezioni del film lacrimale sono spesso sconfortanti.
Lo scopo della terapia varia a seconda della forma di occhio secco:
Lo scopo della terapia varia a seconda della forma di occhio secco:
- nelle forme in cui la causa è la diminuzione del film lacrimale o l'aumento dell'evaporazione, il ricreare il normale spessore lacrimale può essere sufficiente;
- nelle forme cosiddette secondarie, in cui è presente un'altra patologia che altera il film lacrimale, lo scopo della terapia è quello di eliminare la causa principale del disturbo e quindi di utilizzare delle lacrime artificiali in grado di ristabilizzare il film lacrimale diminuendo la sintomatologia per il paziente.
Prima di impostare una terapia d'aiuto al film lacrimale occorre sapere:
- quale parte del film lacrimale è in disordine;
- qual è la causa più verosimile.
Si deve dunque comprendere se l'occhio secco deriva dal deterioramento:
- lipidico;
- acquoso;
- mucinico.
e se dipende da:
- uso di farmaci;
- patologie generali/locali;
- ambienti secchi, VDT, LaC ecc.
L'uso di un sostituto lacrimale deve mantenere buono il visus del paziente e ripristinare il comfort.
Normalmente il pH lacrimale è attorno a 7,2-7,4. Il paziente riferisce sensazione di benessere quando il collirio è alcalino. Normalmente le lacrime artificiali sono a pH tamponato. La frequenza del numero di gocce nella giornata può cambiare a seconda dei momento della malattia e del sostituto lacrimale utilizzato: nelle fasi acute, a volte, è necessaria l'instillazione di sostituti lacrimali ogni ora, mentre nei momenti migliori si può arrivare anche a 4 volte al giorno.
Nella pratica clinica quotidiana si usano molto spesso sostituti lacrimali a seconda della sintomatologia del paziente.
In base alla formulazione e alla loro azione possiamo distinguere le seguenti lacrime:
Normalmente il pH lacrimale è attorno a 7,2-7,4. Il paziente riferisce sensazione di benessere quando il collirio è alcalino. Normalmente le lacrime artificiali sono a pH tamponato. La frequenza del numero di gocce nella giornata può cambiare a seconda dei momento della malattia e del sostituto lacrimale utilizzato: nelle fasi acute, a volte, è necessaria l'instillazione di sostituti lacrimali ogni ora, mentre nei momenti migliori si può arrivare anche a 4 volte al giorno.
Nella pratica clinica quotidiana si usano molto spesso sostituti lacrimali a seconda della sintomatologia del paziente.
In base alla formulazione e alla loro azione possiamo distinguere le seguenti lacrime:
- Diluenti, in grado di allontanare le sostanze prodotte dal metabolismo delle cellule; hanno purtroppo un breve tempo di durata.
- Stabilizzanti, in grado di aumentare la stabilità del film lacrimale.
- Di volume, in cui vi sono sostanze capaci d i legarsi alla superficie oculare e di trattenere acqua.
- Correttive, in grado di correggere alcune caratteristiche fisiche della superficie oculare.
- Nutrienti, che contengono alcune sostanze in grado di migliorare il trofismo dei vari epiteli che sono in sofferenza.
La soluzione chirurgica esiste e può aiutare la superficie oculare a rigenerarsi.
La terapia chirurgica più semplice e più usata nel trattamento delle sindromi da occhio secco consiste nella chiusura, provvisoria o definitiva, dei puntini lacrimali inferiore e/o superiore, per mezzo di piccoli tappi di silicone ("punctum plugs"). Se tale rimedio si dimostra efficace, si ricorre quindi alla chiusura definitiva.
Grazie alle nuove conoscenze nella patogenesi della malattia si è visto che anche l'utilizzo di farmaci anti infiammatori può, in alcuni casi, essere utile e fondamentale per interrompere il meccanismo di patogenesi dei danno.
In particolare negli USA l'FDA ha approvato l'utilizzo di un collirio a base di ciclosporina per trattare i pazienti con occhio secco con un possibile duplice effetto: il primo antiinfiammatorio sulla superficie oculare ed il secondo antiinfiammatorio sulla ghiandola lacrimale che causerebbe un secondario aumento della secrezione lacrimale.
Anche la pilocarpina 1% sistemica, presa per bocca, sembrerebbe essere utile per la stimolazione della secrezione lacrimale nell'occhio e per quella salivare in bocca.
È stato dimostrato che l'assunzione per via orale di preparati contenenti amminoacidi o acidi grassi poli insaturi è in grado di migliorare la sintomatologia e lo stato infiammatorio degli occhi con sindrome da occhio secco e di quelli con occhio secco post chirurgia rifrattiva con laser ad eccimeri.
La terapia chirurgica più semplice e più usata nel trattamento delle sindromi da occhio secco consiste nella chiusura, provvisoria o definitiva, dei puntini lacrimali inferiore e/o superiore, per mezzo di piccoli tappi di silicone ("punctum plugs"). Se tale rimedio si dimostra efficace, si ricorre quindi alla chiusura definitiva.
Grazie alle nuove conoscenze nella patogenesi della malattia si è visto che anche l'utilizzo di farmaci anti infiammatori può, in alcuni casi, essere utile e fondamentale per interrompere il meccanismo di patogenesi dei danno.
In particolare negli USA l'FDA ha approvato l'utilizzo di un collirio a base di ciclosporina per trattare i pazienti con occhio secco con un possibile duplice effetto: il primo antiinfiammatorio sulla superficie oculare ed il secondo antiinfiammatorio sulla ghiandola lacrimale che causerebbe un secondario aumento della secrezione lacrimale.
Anche la pilocarpina 1% sistemica, presa per bocca, sembrerebbe essere utile per la stimolazione della secrezione lacrimale nell'occhio e per quella salivare in bocca.
È stato dimostrato che l'assunzione per via orale di preparati contenenti amminoacidi o acidi grassi poli insaturi è in grado di migliorare la sintomatologia e lo stato infiammatorio degli occhi con sindrome da occhio secco e di quelli con occhio secco post chirurgia rifrattiva con laser ad eccimeri.
Conclusioni
Come tutte le funzioni nel nostro organismo, anche la produzione ed il drenaggio delle lacrime sono sottoposti ad un
rigido equilibrio, che può rompersi a scapito del confort visivo.
La ridotta produzione di lacrime (ipolacrimia), viene per lo più controllata con la continua instillazione di lacrime artificiali; nei casi più resistenti alla terapia utile è l'occlusione dei canalini lacrimali per mezzo di piccoli tappi di materiale sintetico (un tempo erano in argento).
Importante comunque è la prevenzione bevendo sufficienti quantità di liquidi e mantenendo un'adeguata umidità negli ambienti ove abitualmente si vive, specialmente se questi sono asciutti, o riscaldati o raffreddati o ventilati.
La ridotta produzione di lacrime (ipolacrimia), viene per lo più controllata con la continua instillazione di lacrime artificiali; nei casi più resistenti alla terapia utile è l'occlusione dei canalini lacrimali per mezzo di piccoli tappi di materiale sintetico (un tempo erano in argento).
Importante comunque è la prevenzione bevendo sufficienti quantità di liquidi e mantenendo un'adeguata umidità negli ambienti ove abitualmente si vive, specialmente se questi sono asciutti, o riscaldati o raffreddati o ventilati.
La sindrome di Sjögren
a cura di Dr F. Franceschini, Dr.ssa I. Cavazzana - Reumatologia e Immunologia Clinica Ospedali Civili BresciaDefinizione
La Sindrome di Sjögren è una malattia autoimmune sistemica coinvolgente le ghiandole esocrine, caratterizzata da un infiltrato linfoplasmocellulare che conduce alla perdita progressiva della funzionalità ghiandolare.Classificazione
- Primaria: coinvolgimento delle ghiandole esocrine con o senza interessamento sistemico;
- Secondaria: associazione con altre malattie autoimmini (Artrite Reumatoide, LES, Sclerodermia, Vasculiti, Connettiviti...)
Epidemiologia
La prevalenza della Sindrome di Sjögren nella popolazione generale non è stata ancora precisamente valutata: si ritiene che la forma primitiva si presenti con una percentuale dello 0.3-1.5%. Nella popolazione geriatrica è stata stimata una prevalenza del 3% (1).La malattia si manifesta più frequentemente in donne di età compresa tra i 40 e 50 anni (rapporto femmine: maschi di 9:1).
Manifestazioni cliniche
Le manifestazioni cliniche all'esordio possono essere aspecifiche e comparire molti anni prima della diagnosi definitiva.Manifestazioni iniziali di sindrome di Sjögren primaria
Secchezza oculare soggettiva |
47% |
Soggettiva secchezza delle fauci |
42.5% |
Artralgie/ artriti |
28% |
Tumor parotideo |
24% |
Fenomeno di Raynaud |
21% |
Febbre/ astenia |
10% |
Dispareunia |
5% |
Interessamento polmonare |
10.5% |
Interessamento renale |
1.5% |
Interessamento oculare:
i pazienti riferiscono bruciore oculare, prurito, arrossamento, sensazione di corpo estraneo e fotofobia;obiettivamente si rileva un quadro di cheratocongiuntivite secca, non specifico per la Sindrome di Sjögren, ma che deve essere indagata con i seguenti test (facilmente applicabili, ma anche scarsamente specifici perchè possono essere influenzati da diversi fattori quali condizioni ambientali, età, ansia, depressione, uso di psicofarmaci):- Test di Schirmer: valuta il pool lacrimale, tramite una striscia di carta bibula messa a contatto con la ghiandola lacrimale inferiore. Il test risulta positivo se, dopo 5 minuti, la striscia è imbibita meno di 5 mm.
- Break-up Time Test (BUT): si esegue colorando il film corneale con fluoresceina e osservando la sua rottura con lampada a fessura. Valuta quindi l'alterazione del film lacrimale. Un tempo di rottura inferiore a 10 secondi è da considerarsi patologico.
- Rosa Bengala Test il colorante rileva cellule dell'epitelio congiuntivale e corneale danneggiate o con scarsa vitalità. All'osservazione alla lampada a fessura emerge un quadro di cheratite filamentosa o punctata.
Interessamento orofaringeo:
una riduzione della secrezione salivare è responsabile della sensazione di secchezza orale, delle alterazione del gusto, dell'aumento di carie dentarie, che sono riferiti dai pazienti. Nel 60% dei casi si rileva obiettivamente una tumefazione delle parotidi, che all'esordio di malattia, può essere monolaterale e in seguito divenire bilaterale. Vanno escluse altre cause di xerostomia o tumor parotideo, quali: infezioni virali (HIV, HCV), sarcoidosi, neoplasie, endocrinopatie (diabete mellito, acromegalia, iperlipoproteinemie ...), terapia con antiipertensivi o parasimpaticolitici. Vanno eseguite:- Scialografia: si esegue introducendo un mezzo di contrasto idrosolubile nel dotto di Stenone. Si osservano tipicamente scilectasie, restringimenti del dotto di Stenone o dei dotti principali, oppure microcalcificazioni e marcata ritenzione del mezzo di contrasto dopo stimolo acido (succo di limone).
- Biopsia delle ghiandole salivari minori: è altamente specifica per S. di Sjögren se il prelievo comprende 5-10 ghiandole, con il tessuto connettivo circostante; il tessuto presenta infiltrati linfocitari, con un focus score>1.
Manifestazioni extraghiandolari nella sindrome di Sjögren
Artralgie/ artriti |
60-70% |
Fenomeno di Raynaud |
35-40% |
Linfoadenopatia |
15-20% |
Coinvolgimento polmonare |
10-20% |
Coinvolgimento renale |
10-15% |
Vasculite |
5-10% |
Dispareunia |
5% |
Coinvolgimento epatico |
5-10% |
Linfoma |
5-8% |
Neuropatie periferiche |
2-5% |
Miosite |
1-2% |
Apparato osteoarticolare:
Il 60-70% dei pazienti presenta nel corso della malattia episodi di artite, artralgie e morning stiffness.Va eseguita:
- Radiografia Osteoarticolare: che non evidenzia alterazioni erosive.
Interessamento cutaneo:
il fenomeno di Raynaud si presenta nel 35% dei pazienti, accompagnato da un aspetto edematoso delle mani, in assenza di teleangectasie e ulcere digitali. possono manifestarsi anche porpora ipergammaglobulinemica ed eritema anulare.Vanno eseguiti:
- Emocromo con formula e piastrine (in genere anemia normocromica e normocitica e linfo-leucopenia).
- Elettroforesi delle proteine sieriche, con valutazione delle classi anticorpali (in genere ipergammaglobulinemia policlonale specie a carico delle IgG e IgA).
- VES (in genere aumentata).
- Glicemia.
- Crioglobulinemia.
- Complementemia (in genere riduzione di C3 e C4).
- ANA (si ritrovano nelle forme secondarie con specificità della connettivite associata).
- ENA (anti-SSA e anti-SSB sono presenti, spesso insieme, nel 50-70% dei casi di Sindrome di Sjögren primaria).
- Capillaroscopia.
Criteri classificativi
(da Vitali e coll., 1993)Sintomi oculari: una risposta positiva ad almeno una delle seguenti domande:
- Ha una sensazione giornaliera e fastidiosa di secchezza oculare da almeno 3 mesi?
- Ha una sensazione ricorrente di sabbia negli occhi?
- Fa uso di lacrime artificiali più di tre volte al giorno?
- Ha una sensazione giornaliera di secchezza orale da almeno 3 mesi?
- Ha avuto in età adulta episodi ricorrenti e persistenti di tumefazione delle ghiandole salivari?
- E' costretto a bere frequentemente quando mangia cibi secchi?
- Test di Schirmer I (< 5 mm in 5 min).
Questo test non deve essere tenuto in considerazione nei soggetti oltre i 60 anni, ove la riduzione può essere legata all'età. - Test al Rosa Bengala (score >4 secondo van Bijsterveld)
- Scintigrafia salivare
- Scialografia parotidea
- Flusso salivare non stimolato( < 1.5 ml in 15 min).
Questo test non deve essere tenuto in considerazione nei soggetti oltre i 60 anni, ove la riduzione può essere legata all'età.
- anti-Ro (SSA) o La(SSB)
Regole per la corretta classificazione
La presenza di 4 o più criteri in pazienti senza malattie potenzialmente associate alla S. di Sjögren è indicativo di SINDROME DI SJÖGREN PRIMARIA.Nei pazienti con malattie potenzialmente associate alla Sindrome di Sjögren la positività del punto I o II più quella di almeno 2 fra i punti III-VI è probante per una SINDROME DI SJÖGREN SECONDARIA.
Criteri di esclusione
Linfoma persistente, AIDS, sarcoidosi, graft vs host disease, sialoadenosi, uso di antidepressivi, antipertensivi, neurolettici, parasimpaticolitici.Diagnosi differenziale
- altre cause di xerostomia e di xeroftalmia
- forme di Sindrome di Sjögren secondarie
- linfoma
- crioglobulinemia di tipo II, infezione da HCV
- AIDS
Terapia Preventiva
- igiene orale, visite oculistiche periodiche, umidificazione degli ambienti.
Sintomatica
- per il trattamento della secchezza oculare è consigliato l'uso di LACRIME ARTIFICIALI a base di metilcellulosa o di polivinil alcol.
- per il trattamento della secchezza orale è consigliata la frequente assunzione di liquidi, l'uso di spry o gel idratanti del cavo orale.
Sistemica
- FANS
- steroidi a basse dosi
- idrossiclorochina
- immunosoppressori
Bibliografia
Drosos AA, Andonopoulos AP, et al. Prevalence of Primary Sjogren's Syndrome in an elderly population. Br J Rheumatol. 1988; 27: 123-7.torna al menù
Occhio secco e lenti a contatto
a cura di Dott. Manganotti Alberto Medico Chirurgo, Clinica Oculistica Università' di Verona
Cosa si puO' fare
 La comparsa di una alterazione del film lacrimale, soprattutto occhio secco è molto frequente nei vecchi portatori di
LAC morbida.
La comparsa di una alterazione del film lacrimale, soprattutto occhio secco è molto frequente nei vecchi portatori di
LAC morbida. Si calcola che oltre il 80% delle cause di ridotta tollerabilità o intolleranza completa all'uso di LAC sono in qualche modo legate ad un occhio secco indotto dallo stesso uso di LAC mal applicate per molti anni. (dislacrimie secondarie all'uso di lenti a contatto).
E' questo l'aspetto che vorrei rimarcare in questa breve trattazione.
La comparsa di occhio secco, sono talmente frequenti proprio dopo molti anni d'uso di LAC, che vengono spesso erroneamente considerati un evento tipico quasi inevitabile.
Solo una conoscenza delle cause e dei meccanismi che ingenerano queste manifestazioni, consentono, di prevenire tali fenomeni e di permettere l'utilizzo delle lenti in modo soddisfacente per tutta la vita.
Senza entrare nei dettagli di questi meccanismi, basta ricordare che una lente a contatto morbida che si muove poco, produce lentamente la comparsa di dell'occhio secco.
Quindi una LAC morbida si muove poco perché è applicata stretta oppure parchè si disidrata in quanto perde acqua se è già presente occhio è secco (e conseguentemente si "accartoccia" e diventa stretta!!) produce un meccanismo che si autoalimenta (circolo vizioso) che induce occhio secco.
Ovvero: (OCCHIO SECCO + LAC MORBIDA => AUMENTO DELL'OCCHIO SECCO) Tale condizione clinica è nota come "tight lens syndrome" (Sindrome da lente stretta). Più raramente l'iposecrezione lacrimale è legata a condizioni indipendenti dall'uso delle LAC come nel caso delle alterazioni ormonali (le donne in gravidanza che diventano intolleranti, per esempio) o altre malattie generali o oculari.
Deve sospettare la presenza di un iniziale occhio secco chi ha i seguenti disturbi
DURANTE L'USO DELLE LAC:
- appannamenti transitori
- senso di secchezza
- senso di sabbia
- difficoltosa rimozione (effetto ventosa tipico delle lenti morbide)
- necessità di pulire le LAC (più frequente con le lenti rigide)
- annebbiamento serale: tipico annebbiamento complessivo del campi visivo (come in ambiente saturo di vapore) che persiste anche tolte le LAC per circa 5-10 minuti
SENZA USO DELLE LAC:
- fatica ad aprire gli occhi al mattino
- dolore "puntorio" al mattino
- senso di sabbia e lieve secrezione mucosa
- bruciori episodici in condizioni ambientali sfavorevoli, secchi
- iperlacrimazione paradosso: ovvero "colpi" di lacrimazione intensa (come quando si piange).
Cosa possiamo fare se soffriamo di iniziale occhio secco e portiamo LAC morbide?
Anzitutto è necessario fare un vista oculistica (venire senza le LAC ma portandole con se per la valutazione applicativa).L'oculista valuterà la causa, l'entità dell'alterazione del film lacrimale e quindi giudicherà come sono applicate le vostre lenti una volta indossate.
Se le lenti sono strette:
NB: Sospetteremo che una LAC a cambio frequente (usa e getta) possa essere stretta soltanto misurando la cornea: (tutti i soggetti con meridiano corneale medio (Km) più piatto di 41,50 D. (8.13mm), e in cornee di diametro irido-visibile inferiore a 11,3 mm, ovvero hanno gli occhi solo un pò diversi dalla media, sono a rischio di LAC stretta).
... Dovremo applicare LAC SU MISURA!
Se le LAC non sono strette possiamo cambiare il materiale delle LAC usando 4 tipi di materiali:
- HYDROGEL ALLA GLICERINA che hanno una ridotta disidratazione e aumentata reidratazione: sono costruibili SU MISURA ma sono presenti anche a CAMBIO FREQUENTE.
- SILICONE IDROGEL (SI): sono le lenti nate per il porto giorno e nette, hanno una elevata gas permeabilità e una bassa idratazione (si disidratano poco). Ecco le più famose presenti in commercio: Oggi le LAC Silicone Idrogel, possono essere confezionate anche SU MISURA
- OMAFILCON A (fosforilcolina): sono lenti particolarmente "biocompatibili" si disidratano poco e si formano pochi depositi: L'unica disponibile è la Proclear della Cooper Vision presente con LAC GIORNALIERE, MENSILI, (per tutto: miopia astigmatismo e presbiopia) e SU MISURA.
- LAC CON UMETTANTI: sono l'ultima generazione, sempre in evoluzione e molto spinte dal punto di vista pubblicitario: sono generalmente buoni prodotti, è anche possibile provarle gratuitamente.
E se soffriamo di iniziale occhio secco e portiamo LAC RIGIDE?
Anche i portatori di LAC rigide (classiche o gas-permeabili) necessitano di un film lacrimale qualitativamente e quantitativamente buono.Basta pensare che la lacrima deve riempire centralmente gli spazi fra cornea e LAC e che si costituisce sempre un menisco lacrimane al bordo della stessa più significativo, maggiore è il diametro complessivo della LAC. (nella foto la lacrima è colorata con fluoresceina: guardate quanta lacrima "consuma" questa LAC rigida).
La lente ideale per consumare poca lacrima sarà quindi piccola a massima corneoconformità: ovvero la faccia interna deve seguire al massimo la curvatura della cornea.
Per ottenere questo oggi disponiamo della metodica applicativa del CALCO (vedi: le nuove LAC su misura a calco).
Inoltre dalla metà del 2008 abbiamo un nuovo materiale l'Onsifocon A (ONSI-56 by Lagado Com.) che è un silicone idrogel che non assorbe acqua e quindi si comporta come una rigida; si confeziona la LAC come una rigida (con il Calco) ma è il polimero è quello di una morbida molto bagnabile e tollerabile.
Oggi La tecnica applicativa a Calco associata a una corretta scelta del materiale della LAC, consente una tollerabilità elevatissima della LAC rigida, quasi simile a quella di una morbide. Queste lenti si possono considerare una alternativa nei soggetti con occhio secco che non tollerano più le morbide.
CONCLUSIONI:
In presenza di ridotta tollerabilità in un portatore di morbide con occhio secco marginale, "suggeriamo" di provare LAC silicone idrogel, Fosforilcolina, idrogel alla glicerina o quelle con umettanti. Se però valutiamo l'applicazione della LAC morbida stretta, bisogna indicare l'opzione delle lenti su misura con materiali idonei (Fosforilcolina, idrogel alla glicerina e oggi anche silicone idrogel).Dove è indicata l'applicazione di rigida, in presenza di nell'occhio secco iniziale, le LAC rigide custom-made su topografia corneale (LAC a CALCO), sono sempre la prima scelta. Grazie alla elevata tollerabilità di queste lenti, oggi si può considerare una buona alternativa nei soggetti con occhio secco che non tollerano più le morbide.
Test di Schirmer
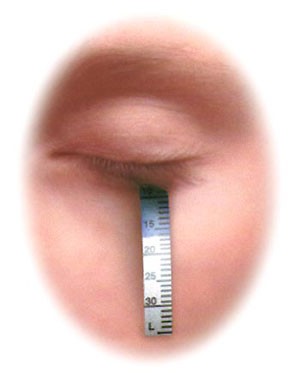 Il test è un indicatore della somma delle così dette secrezioni basale e riflessa.
Si esegue in ambiente poco illuminato, apponendo una cartina nel fornice inferiore al canto esterno e se ne misura
l'impregnazione dopo 5 minuti, avendo il paziente tenuto gli occhi chiusi.
E' stato proposto nel 1903 ma tuttora è il più usato come test di I° livello nella pratica ambulatoriale.
Il test è un indicatore della somma delle così dette secrezioni basale e riflessa.
Si esegue in ambiente poco illuminato, apponendo una cartina nel fornice inferiore al canto esterno e se ne misura
l'impregnazione dopo 5 minuti, avendo il paziente tenuto gli occhi chiusi.
E' stato proposto nel 1903 ma tuttora è il più usato come test di I° livello nella pratica ambulatoriale.Fornisce certamente informazioni interessanti sulla capacità di secrezione lacrimale dell'occhio in esame, tuttavia deve essere condotto con procedure standardizzate in quanto esistono molte variabili che intervengono nel determinare il valore. La più importante variabile deriva dal fatto che l'assorbimento da parte della striscia di carta bibula e la lunghezza della porzione bagnata vengono influenzati dalla forza di capillarità e bagnabilità proprie delle fibre di cellulosa ; ecco perché è importante eseguire il test con cartine validate.
Sebbene il limite dei valori normali sec. Schirmer fosse una impregnazione superiore ai 15mm, oggi si è d'accordo nel definire come franca iposecrezione lacrimale una impregnazione < 5mm/5' ma già pre-patologica a 6 -10mm/5'.
Test della secrezione basale (Test di Jones)
Variante del Test di Schirmer I, fa precedere l'instillazione di una goccia di anestetico locale all'inserimento della cartina, meglio previa asciugatura del fornice inferiore, poi le restanti fasi sono del tutto simili. Valore del Test di Schirmer I -- Valore del Test di Jones = Valore Secrezione riflessa.Test di Schirmer II
Il test è un indicatore della così detta secrezione riflessa. Utilizza la consueta striscia di carta bibula, inserita al fornice inferiore dopo instillazione di anestetico locale. La secrezione riflessa viene stimolata mediante un cotton fioc inserito nella mucosa nasale. Il valore di tale secrezione verrà letto dopo 2'. Valori < 15 mm / 2' sono significativi di una iposecrezione riflessa.Test di Schirmer III
È simile al test di Schirmer II, da cui differisce solo per la sorgente di stimolo della secrezione lacrimale riflessa, che in questo caso è la luce solare.Tralasciando ulteriori varianti proposte in letteratura, i vari test di Schirmer sono forse criticabili soprattutto per le tante variabili in gioco durante le misure; tuttavia, il loro uso nella pratica quotidiana è estremamente utile per la diagnosi corretta delle situazioni di ipolacrimia in molti pazienti, tanto da rendersi indispensabili fintanto che non verrà proposta una valida alternativa che coniughi semplicità e qualità.
mediciitalia.it: occhio secco
Introduzione
L'apparato lacrimale è un sistema interdipendente ( unità funzionale lacrimale U.F.L. ) composto da superfici oculari
(cornea, congiuntiva con le ghiandole in essa
contenute, ghiandola lacrimale ed apparato nervoso afferente ed efferente.
Le fibre efferenti partendo dal Ponte giungono alle ghiandole lacrimali principali ed accessorie, nonchè alle cellule caliciformi congiuntivali ed alle ghiandole di Meibomio.
L'alterazione di uno di questi componenti a livello di questa unità funzionale provoca un malfunzionamento della stessa con la possibilità della comparsa di una sintomatologia anche importante da occhio secco.
Le alterazioni meccaniche corneali, alterano, almeno temporaneamente, l'epitelio e definitivamente la m. di Bowman (plesso subepiteliale!!) e parte dello stroma, con un insulto meccanico delle fibre nervose ed un conseguente rilascio di mediatori chimici.
Tra questi mediatori, vi sono le prostaglandine, e l'effetto antinfiammatorio ed analgesico dei FANS somministrati localmente in caso di danno corneale sarebbe dovuto ad una azione su tali mediatori.
Elementi che possono essere causa di occhio secco. sono l'età, alcuni farmaci (colinergici), malattie sistemiche, alterazioni ormonali ed interventi chirurgici.
I segni sono proporzionali all'entità del problema, e sono arrossamento oculare, cheratiti secche (filamentose, puntate superficiali) fino a veri e propri infiltrati corneali con conseguente compromissione visiva anche definitiva.
Le fibre efferenti partendo dal Ponte giungono alle ghiandole lacrimali principali ed accessorie, nonchè alle cellule caliciformi congiuntivali ed alle ghiandole di Meibomio.
L'alterazione di uno di questi componenti a livello di questa unità funzionale provoca un malfunzionamento della stessa con la possibilità della comparsa di una sintomatologia anche importante da occhio secco.
Le alterazioni meccaniche corneali, alterano, almeno temporaneamente, l'epitelio e definitivamente la m. di Bowman (plesso subepiteliale!!) e parte dello stroma, con un insulto meccanico delle fibre nervose ed un conseguente rilascio di mediatori chimici.
Tra questi mediatori, vi sono le prostaglandine, e l'effetto antinfiammatorio ed analgesico dei FANS somministrati localmente in caso di danno corneale sarebbe dovuto ad una azione su tali mediatori.
Elementi che possono essere causa di occhio secco. sono l'età, alcuni farmaci (colinergici), malattie sistemiche, alterazioni ormonali ed interventi chirurgici.
Segni e sintomi
I sintomi sono bruciori oculari, sensazione di corpo estraneo (ciglia, granello di sabbia), lacrimazione paradossa, dolori puntori, talvolta fotofobia ( importante una anamnesi completa).I segni sono proporzionali all'entità del problema, e sono arrossamento oculare, cheratiti secche (filamentose, puntate superficiali) fino a veri e propri infiltrati corneali con conseguente compromissione visiva anche definitiva.
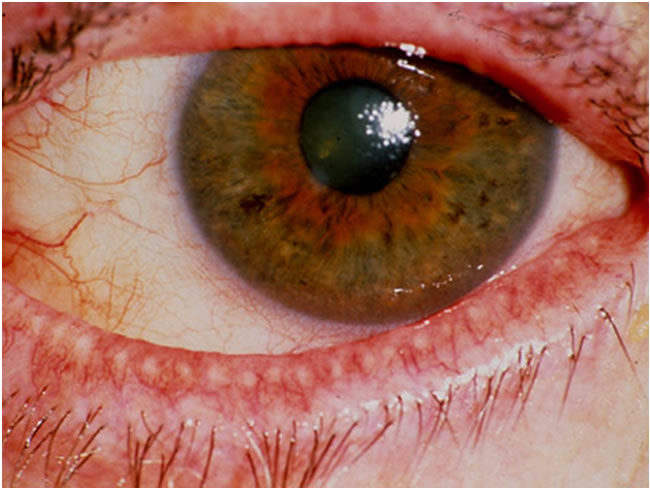 Un classico esempio di occhio secco: notare il riflesso corneale che denota una
secchezza della cornea a causa della scarsità del film lacrimale
Un classico esempio di occhio secco: notare il riflesso corneale che denota una
secchezza della cornea a causa della scarsità del film lacrimale
Quando rivolgersi al medico
In caso di comparsa e persistenza dei sintomi sopra elencati, è necessario
rivolgersi allo specialista per
inquadrare esattamente il tipo di iposecrezione lacrimale (quantitativa e/o qualitativa) e per escludere altre
patologie associate (s. di Sjogren).
Diagnostica
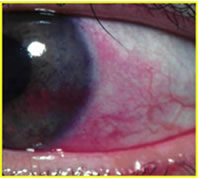 Test di colorazione con rosa Bengala
Test di colorazione con rosa Bengala
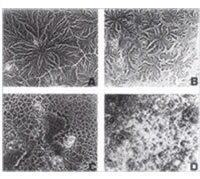 Test di felcizzazione
Test di felcizzazione
Per studiare una situazione di occhio secco esistono esami specifici
- Test di Schirmer ( tipo 1 e tipo 2 )
- Break Up Time
- Test di colorazione con verde di Lissamina
- Test di colorazione con rosa Bengala
- Test di osmolarità del film lacrimale
- Test di colorazione con Fluoresceina
- Test di felcizzazione
- Test di citologia lacrimale
- Fluorescein load test
- Tearscope
- Valutazione funzionalità delle ghiandole di Meibomio
- Imprintig congiuntivale
Terapia
La terapia si basa su sostituti lacrimali che devono avere determinate caratteristichetali da ripristinare l'ambiente
fisiologico del film lacrimale, agendo sulle varie componenti ( mucina, acuosa e lipidica) che lo compongono.
Inoltre devono essere prive di conservanti ( benzlconio cloruro ) che sono fortemente irritanti : a tale proposito devono essere preferiti i sostituti lacrimali in monodose o con sistemi di conservazione di ultima generazione (comod etc.).
Anche l'azione sull'iperosmolarità che è presente nella sindrome da occhio secco risulta essere importante.
Inoltre una terapia innovativa sarà ( quando disponibile in Italia ) la Ciclosporina A.
In caso di infiammazione presente in caso di occhio secco potranno essere di aiuto i FANS locali od anche cortisonici di superficie.
Tutti questi farmaci vanno assunti sempre e comunque sotto la supervisione dello specialista.
Inoltre devono essere prive di conservanti ( benzlconio cloruro ) che sono fortemente irritanti : a tale proposito devono essere preferiti i sostituti lacrimali in monodose o con sistemi di conservazione di ultima generazione (comod etc.).
Anche l'azione sull'iperosmolarità che è presente nella sindrome da occhio secco risulta essere importante.
Inoltre una terapia innovativa sarà ( quando disponibile in Italia ) la Ciclosporina A.
In caso di infiammazione presente in caso di occhio secco potranno essere di aiuto i FANS locali od anche cortisonici di superficie.
Tutti questi farmaci vanno assunti sempre e comunque sotto la supervisione dello specialista.
Prevenzione
In caso di soggetti che hanno la tendenza ad avere la sindrome da occhio secco, sarà importante prevenire le situazioni
che accentuano il problema:
- Ambiente di vita o di lavoro troppo secco (riscaldamento/ raffreddamento con termoconvettori) riscaldamento troppo elevato - scarso ricambio di aria fresca.
- Eccessiva applicazione a videoterminali, che determina una diminuzione della frequenza di ammiccamento.
- Scarso apporto di liquidi con la dieta.
- Evitare squilibri ormonali ( donne in menopausa) od assunzioni di farmaci a base di estroprogestinici senza adeguato controllo.
- Curare i sintomi fin dall'inizio rivolgendosi ad un oculista preparato in materia.
- Seguire con la massima attenzione nel postoperatorio i pazienti operati di chirurgia rifrattiva.
- Proteggere i propri occhi in caso di eccessiva esposizione ai raggi solari o ad agenti atmosferici potenzialmente pericolosi (vento, sabbia etc. ).
Ocular Surface Changes and Discomfort in Patients With Meibomian Gland Dysfunction
Jun Shimazaki, MD; Miki Sakata, MD; Kazuo Tsubota, MDScarica il pdf dell'argomento
Objective: To determine the importance of meibomian gland dysfunction (MGD) on the ocular surface.
Design: Prospective study.
Setting: A university-based referral practice.
Patients: Patients with ocular discomfort (147 eyes) and without ocular discomfort (54 eyes) were examined. In the total 201 eyes, MGD was defined as the presence of an obstruction of the meibomian orifices (obstruction group [n=54]) or the absence of a gland structure (gland dropout group [n=36], or both of these findings (combined group [n=38]). There were not any findings ofMGD in 73 eyes (non-MGD group).
Main Outcome Measures: Scores that were obtainedfrom fluorescein and rose bengal staining, the breakup time of the tear film, the rates of tear evaporation and tear production, and meibography.
Results: Of the 147 eyes with ocular discomfort, 95 (64.6%) had either an obstruction of an orifice or gland dropout, or both. The combined group had higher scores for staining with fluorescein (P=.002) and rose bengal (P=.021) compared with that in the non-MGD group. The rate of tear production was increased more in the gland dropout group than in the non-MGD group (P=.002). The rate of tear evaporation was significantly increased in the gland dropout group (P=.017).
Conclusion: Meibomian gland dysfunction is a major cause of ocular surface abnormalities and ocular discomfort.
(Arch Ophthalmol. 1995;113:1266-1270)
MEIBOMIAN glands secrete lipids into the preocular tear film. These lipids function as a barrier to the in ward movement of skin surface lipids, make the eyelid margin hydrophobic, reduce the evaporation of tears, and lubricate the ocular surface to provide a clear optical image.
Obstructive-type meibomian gland dysfunction (MGD), also called meibomianitis, is characterized by the inspissation of meibomian lipids, resulting in a hyposecretion of lipids in tears. From clinical experiences, MGD has been believed to be one of the major causes of ocular discomfort and abnormalities of the ocular surface.
However, the incidence of MGD in eyes with and without ocular discomfort is not known. Although tear deficiency has been a well-known cause of ocular discomfort, MGD may be another major cause of the symptom. Also, the nature of the changes in the ocular surface and in the tear function of patients with MGD is not fully understood. To determine the importance of MGD on the ocular surface, we prospectively studied the association of the changes in the meibomian gland and that in the ocular surface and tear function.
The involvement of the oily layer of the tear film caused by MGD was investigated by using measurements of tear evaporation.
RESULT - INCIDENCE OF MGD AND ITS ASSOCIATION WITH OCULAR DISCOMFORT
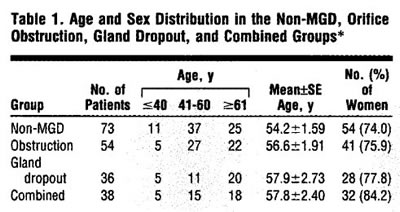 Severe obstruction of the meibomian gland orifice without gland dropout (obstruction group) was identified in 54
of 201 eyes (Table 1). Meibomian gland dropout without obstruction of the orifice (gland dropout group) was present in 36 eyes.
Severe obstruction of the meibomian gland orifice without gland dropout (obstruction group) was identified in 54
of 201 eyes (Table 1). Meibomian gland dropout without obstruction of the orifice (gland dropout group) was present in 36 eyes.Significant obstruction of the orifice and gland dropout were both present in 38 eyes (combined group). No obstruction of the orifice or gland dropout was present in 73 eyes (non-MGD group). There were no differenees in the mean age and sex distribution among these groups (Table 1).
In 147 of the total 201 eyes, there were symptoms (eg, foreign-body sensation, conjunctival injection, and photophobia) of ocular discomfort. In 54 eyes, there were not any symptoms of ocular discomfort. Among 147 eyes of patients with ocular discomfort, there was tear deficiency in 53 (36.1%). In 95 (64.6%) of these 147 eyes, there was either an obstruction of the orifice or gland dropout (Table 2).
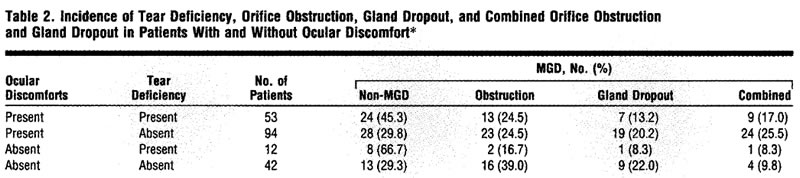
In 94 eyes with ocular discomfort that had normal tear secretion, 70 (74.5%) had either an obstruction of the orifice or gland dropout, or both of these changes. The incidence of combined changes of obstruction of the orifice and gland dropout in eyes with ocular discomfort was significantly higher than those without discomfort (33 [22.4%] vs five [9.3%] eyes, P=.03).
PATIENTS AND METHODS
PATIENTS
One hundred forty-seven eyes in 82 patients with ocular discomfort (14 men and 68 women; mean±SD age, 54.4± 14.2 years) and 54 eyes without ocular discomfort in 29 patients (11 men and 18 women; mean±SD age, 61.2±14.2 years) were analyzed in this study. The relation between meibomian gland function and changes in ocular surface and tear function in the total 201 eyes in the 111 patients was studied. We excluded from the study any patients with eyes with disorders that could have affected the ocular surface (eg, patients with infectious conjunctivitis, diabetes mellitus, allergic diseases, autoimmune diseases, and collagen diseases, and users of preservativecontaining eyedrops).Patients whose eyes had excessive meibomian lipid secretion (seborrheic MGD) were also excluded, in that seborrheic MGD is a distinct clinical entity.
ASSESSMENT OF OCULAR SURFACE CHANGES
To determine the presence of damage to the conjunctival and corneal epithelia, we instilled 2 µ of mixtures (1:1) of preservative-free-staining solutions that consisted of 1% fluorescein (Fluorescite injection, Alcon Japan Co, Tokyojapan) and 1% rose bengal powder (Rose Bengal, Wako Pure Chemical Industries Ltd, Osaka, Japan) dissolved in saline solution.Results were assessed semiquantitatively by using a grading scale for fluorescein staining in the cornea (range of grades, 0 to 3) and a scale for rose bengal staining in both the cornea and conjunctiva (range of grades, 0 to 9), according to previously described methods.
The breakup time of the tear film was subsequently measured three times. The average of these three measurements is presented in the "Results" section. Subjective symptoms of these patients were examined by a questionnaire as described previously.
EXAMINATION OF TEAR FUNCTION
The rate of tear secretion was determined by using Schirmer's test after the application ofa topical anesthetic agent (0.4% benoxinate hydrochloride [oxybuprocaine hydrochloride] [Benoxil], Santen Pharmaceutical Co, Osaka, Japan). Tear deficiency was defined as a wet length (5 mm) on a test strip by using Schirmer's test. The tear clearance test was performed at the same time as Schirmer's test by evaluating the dilution rate of fluorescein, which was instilled 5 minutes before Schirmer's test was performed. Clearance was definedaslX,2X,4X,8X,16X,32X,64X,128X,and256X.The logarithm of the result was used as a parameter for tear dynamics. We also performed the cotton thread test to measure the amount of tears in the tear meniscus.8 The rate of tear evaporation was measured in selected patients by using a previously reported method.
The tear evaporation rate at 40% humidity was used as a representative number of the measurement.
ASSESSMENT OF MEIBOMIAN GLAND FUNCTION
We used two techniques for evaluating meibomian gland function: (1) observation of meibomian gland orifices by using biomicroscopy and (2) transillumination observation techniques by using a light probe (meibo-[molgraphy).We did not use the volume and viscosity scales of meibomian gland expression" because we found that lipid secretion varied among meibomian orifices and depended on the day on which measurements were obtained. We there fore used a simplified criterion to determine the decrease in meibomian secretions. The lack of secretion following the application of moderate digital pressure on the tarsus of the upper eyelid was considered as a decrease in the secretion.
The procedure was performed by a single investigator Q.S.), who attempted to apply a constant pressure during the study. Temperature and humidity of the examination room were maintained at a range from 15°C to 20°C and 30% to 50%, respectively. Meibography was performed by using a transillumination device for vitrectomy with a fiberoptic light source (L-3920, Inami Co, Tokyojapan) with a 20-gauge disposable fiber light guide.14 This device presents advantages over a conventional transilluminator in that the fine tip of the light guide can be hidden behind an everted eyelid, making it possible to observe gland structure without interference from a bright light.
Loss of visible meibomian gland structure ("gland dropout") has been observed in patients with severe MGD.121416 Therefore, the presence of gland dropout at the central two thirds of the lower tarsus indicated the presence of MGD in this study.
Observations and tests were conducted in the following order to avoid the influence of one procedure on another: tear evaporation, rose bengal and fluorescein staining, breakup time of the tear film, cotton thread test, Schirmer's test, tear clearance test, meibography, and, finally, evaluation of meibomian secretion.
In some patients, the evaporation of tears was determined on a different day from that of the other examinations.
STATISTICAL ANALYSIS
Data are presented as mean±SE. Between-group differences in the mean age, breakup time of the tear film, Schirmer's test, tear clearance test, cotton thread test, and tear evaporation rate were evaluated by using the one-way analysis of variance test.The Mann-Whitney U test was used to evaluate differences in the results of the scores for the fluorescein and rose bengal staining. Differences in the incidence was evaluated by using the 2 test.
MEIBOMIAN GLAND FUNCTION AND OCULAR SURFACE CHANGES
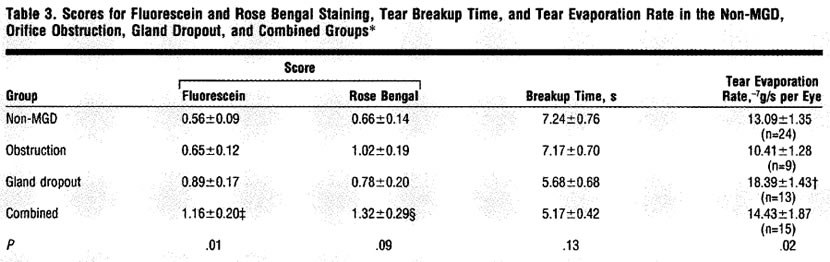 The score for fluorescein staining was correlated with the presence of obstruction of the orifice and gland dropout
(Table 3, P=.01). Scores for fluorescein and rose bengal staining were higher in the combined group than in the non-MGD group
(P=.002 and P=.021, respectively).
The score for fluorescein staining was correlated with the presence of obstruction of the orifice and gland dropout
(Table 3, P=.01). Scores for fluorescein and rose bengal staining were higher in the combined group than in the non-MGD group
(P=.002 and P=.021, respectively).There were no significant differences in the scores for the fluorescein and rose bengal staining between the non-MGD and obstruction groups. Breakup times of the tear film were shorter in the dropout and combined groups than in the non-MGD group; however, the differences were not statistically significant (P=.19 and P=.06, respectively).
The rates of tear evaporation were measured in 61 eyes in 31 patients (eight men and 23 women; mean±SD age, 52.3± 13.8 years) with and without MGD. The mean±SE rate of tear production, measured by using Schirmer's test, was 10.1 ±1.0 mm/5 min in these 61 eyes.
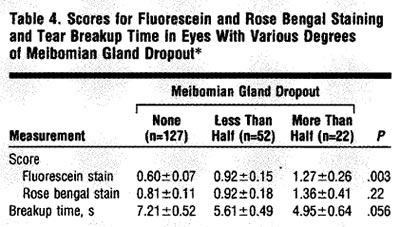 The rates of tear evaporation were significantly different among the groups (Table 3, P=.02).
The rates of tear evaporation were significantly different among the groups (Table 3, P=.02). The rate in the gland dropout group was significantly increased compared with that in the non- MGD group (P=.017). The rates of tear evaporation in the obstruction group and combined group were not different significantly with those in the non-MGD group.
Meibography showed variations in gland destruction that ranged from the dropout of a single gland structure to a total destruction. In the present study, the score for fluorescein staining was correlated with the degree of gland dropout (Table 4, P=.003). The score for rose bengal staining and the breakup time of the tear film also changed as the severity of gland dropout increased, although they did not reach statistically significant levels (Table 4).
MEIBOMIAN GLAND AND TEAR FUNCTION
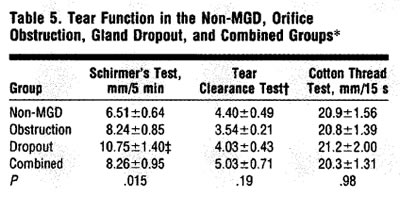
The tear production, as measured by using Schirmer's test, was significantly increased in the gland dropout group compared with that in the non-MGD group (P=.002).Results of the cotton thread and tear clearance tests did not differ among the groups (Table 5).
COMMENT
 By using the criteria of obstruction of the orifice or gland dropout, we identified MGD in 95 (64.6%) of 147 eyes with symptoms of
ocular discomfort (Table 2). In eyes with normal tear secretion, abnormalities in the meibomian gland were attributed to more than
two thirds (74.5%) of the ocular discomfort. One of us (K.T.)17 defined "dry eye" as "a disorder which causes abnormalities of the
ocular surface by changing the quality and/or quantity of tears"; thus, MGD is the major cause of dry eye as well as tear deficiency.
By using the criteria of obstruction of the orifice or gland dropout, we identified MGD in 95 (64.6%) of 147 eyes with symptoms of
ocular discomfort (Table 2). In eyes with normal tear secretion, abnormalities in the meibomian gland were attributed to more than
two thirds (74.5%) of the ocular discomfort. One of us (K.T.)17 defined "dry eye" as "a disorder which causes abnormalities of the
ocular surface by changing the quality and/or quantity of tears"; thus, MGD is the major cause of dry eye as well as tear deficiency.
Disorders of the ocular surface were found to be more severe in the eyes with significant obstruction of the meibomian orifice and gland dropout compared with those in the eyes without MGD (Table 3).
Scores for fluorescein and rose bengal staining reflected the damage of the ocular surface, indicating that these were appropriate parameters for evaluating MGDrelated ocular surface changes. We found the rate of tear production to be higher in the gland dropout group than in the non-MGD group (Table 5).
This finding is in contrast to that found in a previous report that described tear deficiency as being often associated with MGD. Although the reason for the difference is unknown, increased rates of tear production were also noted in the obstruction and combined groups, suggesting that this finding is not incidental. This may be a compensation for the abnormality of the ocular surface, or a result of increased reflex tearing. The fact that more severe changes were seen in the ocular surface in the obstruction, gland dropout, and combined groups, despite an increase in tear secretion, indicated that a change in meibomian function, rather than an abnormality in tear function, was responsible for the changes that were observed.
Although the effects of MGD on the ocular surface have been recognized clinically, no previous report, to our knowledge, has shown that MGD produces changes in the ocular surface.
We found that the rate of tear evaporation was increased in the gland dropout group (Table 3). This suggests that changes in the oily layer of the tear film occurs in MGD. This finding is in good accordance with that found in the study by Mathers,15 who reported that the numbers of gland dropout were correlated with the increase in the rate of tear evaporation.
The absolute value for tear evaporation in the MGD group was considerably smaller in our study than in that of Mathers,15 perhaps because of the differences in the methods that were used. Another explanation for the increased rate of tear evaporation in the gland dropout group could have been that these eyes had more of a tear reservoir on their ocular surface, as indicated by the results of Schirmer's test.
This appeared to be unlikely, however, since the values of the cotton thread test, which reflects the amount of tears in the inferior cul-de-sac, were not different in the gland dropout and non-MGD groups (Table 5).
Clinically, MGD is characterized by a stagnation of meibomian secretion. Obstruction of a meibomian gland duct is caused by either keratinization of the duct or qualitative changes in the meibomian lipids.
A previous histological study of MGD has revealed an obstruction and dilatation of the ducts, enlargement of acini, foreign reactions, and, in an advanced stage, a total destruction of the gland structure. The gland dropout that was detected by using meibography was believed to show a destruction of the meibomian gland structure.
Therefore, gland dropout is more likely to represent more severe changes in the meibomian gland than in the obstruction of the orifice. The score for fluorescein staining and the rate of tear evaporation were higher in the gland dropout group than in the obstruction group in the present study; these findings are consistent with this theory. These changes in the ocular surface were more severe in the eyes with gland dropout in more than half of the tarsus of the inferior eyelid than in those with the gland dropout in less than half of that region (Table 4).
It is likely that at some critical point the other vital glands are unable to compensate for the impairment of meibomian gland function. Although both biomicroscopy and meibography are useful for assessing MGD, meibography appears to be more appropriate because it is more stable, is less subject to interobserver variation, and allows for a semiquantitative assessment.
In summary, our results showed that MGD is one of the major causes of ocular discomfort and abnormality in the ocular surface. Tear deficiency may or may not be accompanied with the disorder. An excessive evaporation of tears may have been responsible for the changes that were observed. The results of the meibomian orifice observation and meibography were associated with the severity of the changes in the ocular surface.
The procedures that were used in the present study are convenient for clinical use and provide reproducible results without requiring expensive instruments or special techniques.
Accepted for publication May 16, 1995. Reprint requests to Department of Ophthalmology, Tokyo Dental College, 5-11-13 Sugano, Ichikawa-shi, Chiba, 272 Japan (Dr Shimazaki).
torna al menù
Data ultimo aggiornamento pagina: 16/11/2012

